题目内容
14.向一定质量的硝酸银和硝酸铜的混合溶液中加入m克锌粉,充分反应后过滤,将滤渣洗涤、干燥后称量,得到的固体质量为m克,据此,下列说法不正确的是( )| A. | 滤渣中的物质至少有两种 | |
| B. | 取反应后的滤液观察,滤液可能呈蓝色 | |
| C. | 去反应后的滤液滴加稀盐酸,无白色沉淀产生 | |
| D. | 向滤渣滴加稀盐酸,一定有气泡产生 |
分析 根据金属与盐溶液的反应进行分析,在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,且置换时先把最弱的金属置换出来,并通过固体质量不变化分析.
解答 解:在金属活动性顺序中,Zn>Cu>Ag,向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,与两种溶质依次发生反应:
Zn+2AgNO3=Zn(NO3)2+2Ag
65 216
所以析出银的过程是固体质量增加的过程;
Zn+Cu(NO3)2=Zn(NO3)2+Cu
65 64
所以析出铜的过程是固体质量减少的过程;
而反应前后固体质量都是mg,说明硝酸银被置换完了,硝酸铜也发生了置换反应,因此滤渣一定含有银和铜,可能含有锌;滤液一定含有硝酸锌,可能含有硝酸铜,一定没有硝酸银;
A、滤渣一定含有银和铜,可能含有锌,故说法正确.
B、滤液可能含有硝酸铜,因此滤液可能呈现蓝色,故说法正确;
C、由于硝酸银完全被置换出来,取反应后的滤液滴加稀盐酸,没有沉淀产生,故说法正确;
D、因为滤渣可能含有锌,因此取滤渣滴加盐酸,可能有气泡,故说法错误.
故选:D.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序的意义结合实验的现象进行分析得出结论.

练习册系列答案
相关题目
4.下列常见溶液为无色的是( )
| A. | 高锰酸钾溶液 | B. | 酚酞溶液 | C. | 石蕊溶液 | D. | 氯化铁溶液 |
5.亮亮做家务时接触到下列用品.
(1)他清理垃圾时发现一袋脱氧剂,拆开后看到还原铁粉已生锈,铁生锈的原因是Fe与潮湿的空气接触.
(2)不能用洁厕灵清理生锈铁制品,用化学方程式表示其原理Fe+2HCl═FeCl2+H2↑.
(3)他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是NaOH有强腐蚀性.
(4)炉灶清洁剂敞口放置易变质失效,用化学方程式表示其原理2NaOH+CO2═Na2CO3+H2O.
| 用品 | 脱氧剂 | 洁厕灵 | 炉灶清洁剂 |
| 有效成分 | 还原铁粉 | 盐酸 | 氢氧化钠 |
(2)不能用洁厕灵清理生锈铁制品,用化学方程式表示其原理Fe+2HCl═FeCl2+H2↑.
(3)他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是NaOH有强腐蚀性.
(4)炉灶清洁剂敞口放置易变质失效,用化学方程式表示其原理2NaOH+CO2═Na2CO3+H2O.
 已知A-E是初中化学的常见物质.A和D是两种常见的碱,B是一种常见的酸,且只含有两种元素,C是一种钠盐.它们相互间转化或发生反应的关系如图所示.
已知A-E是初中化学的常见物质.A和D是两种常见的碱,B是一种常见的酸,且只含有两种元素,C是一种钠盐.它们相互间转化或发生反应的关系如图所示.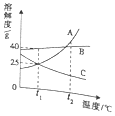 水与人类的生活和生产密切相关.请根据信息回答.
水与人类的生活和生产密切相关.请根据信息回答.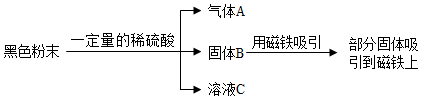 取含有铁粉、氧化铜、银粉(黑色)三种物质组成的黑色粉末进行实验,流程如图:
取含有铁粉、氧化铜、银粉(黑色)三种物质组成的黑色粉末进行实验,流程如图: