题目内容
17.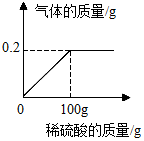 生铁和钢都是铁合金,生铁中碳的含量在2.0%~4.3%之间,钢中碳的含量在0.03%~2%之间.某兴趣小组同学取铁合金样品5.7g(假设只含铁单质及碳单质),加入稀硫酸至不再产生气体为止,反应过程中生成的气体与所加稀硫酸酸的质量关系如图所示.根据计算回答(计算结果保留一位小数):
生铁和钢都是铁合金,生铁中碳的含量在2.0%~4.3%之间,钢中碳的含量在0.03%~2%之间.某兴趣小组同学取铁合金样品5.7g(假设只含铁单质及碳单质),加入稀硫酸至不再产生气体为止,反应过程中生成的气体与所加稀硫酸酸的质量关系如图所示.根据计算回答(计算结果保留一位小数):(1)该铁合金是生铁还是钢?
(2)加入的稀硫酸中溶质的质量分数?
分析 生铁和钢都是铁合金,铁可以与硫酸反应,碳不反应,利用化学方程式,根据氢气的质量求铁和硫酸的质量,及一步计算碳的含量和稀硫酸中溶质的质量分数.
解答 解:设样品中铁的质量为x,加入的稀硫酸中溶质的质量为y,
Fe+H2SO4═FeSO4+H2↑
56 98 2
x y 0.2g
$\frac{56}{x}=\frac{98}{y}=\frac{2}{0.2g}$
解得:x=5.6g,y=9.8g,
(1)样品中碳的质量分数为:$\frac{5.7g-5.6g}{5.7g}$×100%=1.8%<2%,
因此该铁合金是钢;
(2)加入的稀硫酸中溶质的质量分数:$\frac{9.8g}{100g}×100%$=9.8%;
答:加入的稀硫酸中溶质的质量分数为9.8%;
故答案为:(1)钢(2)9.8%.
点评 本题主要考查有关化学方程式的计算和质量分数的计算,根据质量守恒定律求反应后所得溶液的质量是重点,要牢固把握.

练习册系列答案
相关题目
7.下列叙述中,不正确的是( )
| A. | 原子的质量主要集中在原子核上 | |
| B. | 直接构成物质的粒子有分子、原子和离子 | |
| C. | 在公园散步闻到花的香味是因为分子在不停地运动 | |
| D. | 给篮球打气时气体被压缩,分子变小了 |
8.下列关于能源的叙述正确的是( )
| A. | 人类需要的能量都是由化学反应产生的 | |
| B. | 煤和石油都是可再生能源 | |
| C. | 大气污染,因此使用天然气可以避免污染 | |
| D. | 目前没有大量使用氢能源,是由于氢气的制取成本高,储存困难 |
12. 如图是A、B、C三种固体物质的溶解度曲线.下列分析不正确的是( )
如图是A、B、C三种固体物质的溶解度曲线.下列分析不正确的是( )
 如图是A、B、C三种固体物质的溶解度曲线.下列分析不正确的是( )
如图是A、B、C三种固体物质的溶解度曲线.下列分析不正确的是( )| A. | 将50℃时A、B的饱和溶液降温至20℃,析出晶体质量A不一定大于B | |
| B. | 50℃时,把50gA放入50g水中,形成的溶液其中溶质与溶剂的质量比为1:2 | |
| C. | 将C的饱和溶液变为不饱和溶液,可采用降温的方法 | |
| D. | 分别将三种物质的饱和溶液从50℃降至20℃时,所得溶液溶质质量分数大小关系是B>C=A |
2.2015年10月5日浙江绍兴一化工厂因硝基氯苯车间反应引起爆炸.硝基氯苯化学式C6H4ClNO2,关于硝基氯苯的说法正确的是( )
| A. | 硝基氯苯中氢元素的质量分数比氮元素大 | |
| B. | 硝基氯苯是由碳、氢、氯、氮、氧五种元素组成 | |
| C. | 硝基氯苯是属于氧化物 | |
| D. | 硝基氯苯是由6个碳原子、4个氢原子、1个氯原子、1个氮原子和2个氧原子构成 |
9.如图是某密闭容器中物质变化的微观示意图,其中“●”代表氧原子,“○”代表硫原子,下列说法不正确的是( )


| A. | 变化Ⅱ中参加反应的和生成的三种分子 的个数比为2:1:2 的个数比为2:1:2 | |
| B. | 变化Ⅱ发生的是分解反应 | |
| C. | 变化Ⅰ中的“一定条件”可能是升高温度 | |
| D. | 变化Ⅱ后所得物质为混合物 |
6.根据你的生活经验和所学知识,判断下列做法不能达到目的是( )
| A. | 用食盐水除去水垢 | |
| B. | 用肥皂水鉴别硬水和软水 | |
| C. | 用含氢氧化铝的药物治疗胃酸过多 | |
| D. | 用在空气中灼烧的方法鉴别黄铜和黄金 |
7.地球上可利用的淡水不到总水量的1%,我们应爱护水资源.下列有关水的说法正确的是( )
| A. | 海水都是混合物,淡水都是纯净物 | |
| B. | 通过水的电解实验可以得到“水是由氢气和氧气组成”的结论 | |
| C. | 爱护水资源主要应从节约用水和防治水体污染两方面采取措施 | |
| D. | 硬水是含有可溶性钙、镁化合物的水,软水是不含可溶性钙、镁化合物的水 |