题目内容
12. 如图是A、B、C三种固体物质的溶解度曲线.下列分析不正确的是( )
如图是A、B、C三种固体物质的溶解度曲线.下列分析不正确的是( )| A. | 将50℃时A、B的饱和溶液降温至20℃,析出晶体质量A不一定大于B | |
| B. | 50℃时,把50gA放入50g水中,形成的溶液其中溶质与溶剂的质量比为1:2 | |
| C. | 将C的饱和溶液变为不饱和溶液,可采用降温的方法 | |
| D. | 分别将三种物质的饱和溶液从50℃降至20℃时,所得溶液溶质质量分数大小关系是B>C=A |
分析 A、不知饱和溶液的质量,无法判断析出晶体的质量多少;
B、根据50℃时,A的溶解度为50g,即50℃时,100g水中溶解50gA物质达到饱和进行解答;
C、根据溶解度曲线可知,C的溶解度随温度的升高而降低进行解答;
D、根据三种物质的溶解度随温度变化及饱和溶液中溶质的质量分数计算式分析解答.
解答 解:A、不知二者饱和溶液的质量,所以将50℃时A、B的饱和溶液降温至20℃,析出晶体质量A不一定大于B,故A正确;
B、50℃时,A的溶解度为50g,即50℃时,100g水中溶解50gA物质达到饱和,所以50℃时,A的饱和溶液中溶质与溶剂的质量比为=50g:100g=1:2,故B正确;
C、根据溶解度曲线可知,C的溶解度随温度的升高而降低,所以将C的饱和溶液变为不饱和溶液,可采用降温的方法,故C正确;
D、AB的溶解度随温度降低而减小,C的溶解度随温度的降低而增大,所以分别将三种物质的饱和溶液从50℃将至20℃时,AB析出晶体,依然是饱和溶液,此时B的溶解度大于A,C变为不饱和溶液,溶质的质量分数与降温前相等,20℃时A的溶解度与C的溶解度相等,根据饱和溶液中溶质的质量分数的计算式$\frac{溶解度}{溶解度+100g}$×100%可知:降温后所得溶液溶质质量分数大小关系是B>A>C,故D错误;
故选:D.
点评 掌握溶解度的概念、溶解度曲线的意义及溶质的质量分数计算方法,并能结合选项灵活分析解答问题.

练习册系列答案
相关题目
2.下列科研项目属于化学研究范畴的是 ( )
| A. | 研究杂交水稻,提高产量 | B. | 研制出新型防水材料 | ||
| C. | 研究提高水利发电机的效率 | D. | 研制新型机器人为人民服务 |
20.某物质在空气中燃烧的化学方程式为X+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O,下列说法正确的是( )
| A. | X的化学式为C2H4 | |
| B. | 该反应属于置换反应 | |
| C. | CO2中氧元素的化合价为-2 | |
| D. | 反应前后分子原子的种类均未发生改变 |
1.厨房中安装燃气报警器可用于检测燃气是否泄漏.从分子角度解释,这是因为( )
| A. | 分子体积很小 | B. | 分子不断运动 | C. | 分子间有间隔 | D. | 分子可以再分 |
2.生活与化学紧密相连,以下叙述中发生化学变化的是( )
| A. | 冰块融化 | B. | 桂花飘香 | C. | 饭菜变馊 | D. | 铸铁成锅 |
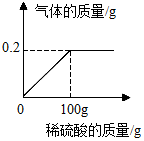 生铁和钢都是铁合金,生铁中碳的含量在2.0%~4.3%之间,钢中碳的含量在0.03%~2%之间.某兴趣小组同学取铁合金样品5.7g(假设只含铁单质及碳单质),加入稀硫酸至不再产生气体为止,反应过程中生成的气体与所加稀硫酸酸的质量关系如图所示.根据计算回答(计算结果保留一位小数):
生铁和钢都是铁合金,生铁中碳的含量在2.0%~4.3%之间,钢中碳的含量在0.03%~2%之间.某兴趣小组同学取铁合金样品5.7g(假设只含铁单质及碳单质),加入稀硫酸至不再产生气体为止,反应过程中生成的气体与所加稀硫酸酸的质量关系如图所示.根据计算回答(计算结果保留一位小数):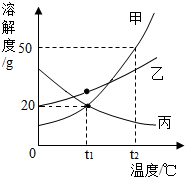 如图为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线.
如图为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线.