题目内容
2.“3CO2”与“6CO”中具有相同的是( )| A. | 分子个数 | B. | 碳元素的质量分数 | ||
| C. | 氧原子个数 | D. | 碳与氧元素的质量比 |
分析 根据CO和CO2的元素组成,分子构成和性质进行判断,二者的都是由碳氧元素组成的,每个分子中所含原子个数不同,元素的质量比就不同,根据元素的质量分数=$\frac{元素的相对原子质量×原子个数}{物质的相对分子质量}$×100%,判断元素质量分数是否相同.
解答 解:A、“3CO2”与“6CO”中分子个数不相等;不正确;
B、一氧化碳中碳元素的质量分数=$\frac{12}{12+16}$×100%=≈43%,二氧化碳中碳元素的质量分数=$\frac{12}{12+16×2}$×100%≈27%,碳元素质量分数不同,故错误;
C、“3CO2”与“6CO”中氧原子个数相等,故C正确;
D、“3CO2”中碳与氧元素的质量比:(3×12):(3×16×2)=3:8;“6CO”中碳与氧元素的质量比(12×6):(6×16)=3:4,故D不正确.
故选C.
点评 本题考查的是学生对化学式的认知情况,有利于学生对这部分知识的整体认知.

练习册系列答案
相关题目
13.一天晚上,小明看见妈妈用热的纯碱溶液清洗餐具上的油污.餐具在放入溶液中后上面的油污立即“消失”.小明对其中的原理产生了好奇,并展开探究.
(1)首先,小明对纯碱溶液清洗油污的原理做出如下猜想:①像水中加入纯碱(化学式是Na2CO3)增大了油污在水中的溶解度,此过程只发生了物理变化.②热的碱性溶液使油污发生反应.
(2)为了验证猜想,小明配置了一定浓度的热纯碱溶液,向其中加入适量食用油(可忽略溶液体积变化),然后用PH计分别测定加入食用油前后溶液的PH变化,发现pH减小,可初步推断溶液中发生了化学反应.
(3)查阅资料得知,热的纯碱溶液可以使油污水解,生成易溶于水盐类物质和醇类物质.于是,小明开始探究溶液去污能力与碱性强弱的关系.首先他配置了等量等浓度的三种碱溶液,然后分别加入适量的食用油,测量并记录食用油溶解所需时间.下面是小明实验记录表格.
序号【4】应填入80℃,Na2CO3溶液15ml,根据小明的实验,可以得到的结论是溶液碱性越强,去污能力越强.
(1)首先,小明对纯碱溶液清洗油污的原理做出如下猜想:①像水中加入纯碱(化学式是Na2CO3)增大了油污在水中的溶解度,此过程只发生了物理变化.②热的碱性溶液使油污发生反应.
(2)为了验证猜想,小明配置了一定浓度的热纯碱溶液,向其中加入适量食用油(可忽略溶液体积变化),然后用PH计分别测定加入食用油前后溶液的PH变化,发现pH减小,可初步推断溶液中发生了化学反应.
(3)查阅资料得知,热的纯碱溶液可以使油污水解,生成易溶于水盐类物质和醇类物质.于是,小明开始探究溶液去污能力与碱性强弱的关系.首先他配置了等量等浓度的三种碱溶液,然后分别加入适量的食用油,测量并记录食用油溶解所需时间.下面是小明实验记录表格.
| 序号 | 溶液 | 碱性强弱 | 食用油完全溶解时间 |
| 【1】 | 25°C,NaHCO3溶液15ml | 最弱 | 10S |
| 【2】 | 25°C,Na2CO3溶液15ml | 较弱 | 8S |
| 【3】 | 70°C,Na2CO3溶液15ml | 较强 | 4S |
| 【4】 | ? | 最强 | 2S |
7.下列实验方法中,不能达到实验目的是( )
| A | 用过滤的方法除去黄河水中的泥沙 |
| B | 用水鉴别硫酸铜固体和氢氧化钠固体 |
| C | 用BaCl2溶液中除去NaCl溶液中的Na2CO3杂质 |
| D | 用燃着的木条鉴别二氧化碳和氮气 |
| A. | A | B. | B | C. | C | D. | D |
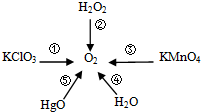 如图所示,很多物质分解可以产生氧气.
如图所示,很多物质分解可以产生氧气.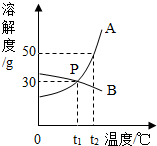 如图是A、B两种物质的溶解度曲线,右图是A、B的溶解度曲线.P点意义为t1℃时AB的溶解度相等;把t2℃时150gA的饱和溶液稀释为20%,需加水100gg.
如图是A、B两种物质的溶解度曲线,右图是A、B的溶解度曲线.P点意义为t1℃时AB的溶解度相等;把t2℃时150gA的饱和溶液稀释为20%,需加水100gg. 随意丢弃废旧干电池会造成环境污染,而废旧干电池中的许多物质都是可以回收利用的.请根据如图回答下列问题:
随意丢弃废旧干电池会造成环境污染,而废旧干电池中的许多物质都是可以回收利用的.请根据如图回答下列问题: