题目内容
5.汇仙湖公园有丰富的负氧离子,空气中氧分子(O2)得到电子就能形成负氧离子(O2-).一个负氧离子与一个氧分子比较,不相同的是( )| A. | 电子数 | B. | 质子数 | ||
| C. | 含氧原子个数 | D. | 相对原子质量之和 |
分析 由题意可知:“空气中氧分子得到电子就能形成负氧离子”,由此可得该粒子的形成过程,从电子的得失以及微粒的结构等方面分析解答即可.
解答 解:A、通过O2-与O2比较,O2得到了1个电子后形成离子O2-,所以O2-与O2电子数不相同,故说法符合题意;
B、通过O2-与O2比较,两微粒间的转化质子数并没有发生改变,所以可知O2-与O2质子数相同,故说法不符合题意;
C、通过O2-与O2比较,可知O2-与O2含氧原子个数相同,故说法不符合题意;
D、通过O2-与O2比较,因变化前后质子数和中子数都不变,则相对原子质量也不变,可知O2-与O2相对原子质量之和相同,故说法不符合题意;
故选A.
点评 解答时了解原子和离子的相互转化,变化的是电子,了解原子的构成和特定的,掌握相对原子质量的计算方法即可正确解答.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
13. 甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
 甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | 两种物质的溶解度都随着温度的升高而增大 | |
| C. | t1℃时,60g甲加入到100g水中,充分溶解,得到160g溶液 | |
| D. | 甲、乙的饱和溶液从t2℃降温到t1℃,析出晶体的质量:甲一定小于乙 |
20.下列关于“生活中的化学”的叙述中,不正确的是( )
| A. | 胃酸过多可服用适量的小苏打 | |
| B. | 油锅着火可以立即用冷水浇灭 | |
| C. | 食用加碘食盐可预防甲状腺肿大 | |
| D. | 水中的色素和异味可以用活性炭除去 |
10.如表是固体A、B、C在不同温度时的溶解度.
(1)若饱和溶液B中混有少量的A,最好采用降温结晶的方法提纯B.
(2)将80℃时A、B、C三种物质的饱和溶液降温到60℃,其中溶质质量分数不变的物质是C.
(3)精制A时,通常采用的是蒸发溶剂的方法而不用降低溶液温度的方法,请据表分析,其原因是A的溶解度受温度影响不大.
(4)20℃时,溶解3.5g的固体C,蒸馏水的最佳使用量约为10ml.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 固体A | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| 固体B | 13.3 | 31.6 | 63.9 | 110 | 169 | |
| 固体C | 35.0 | 44.5 | 57.6 | 55.0 | 50.0 |
(2)将80℃时A、B、C三种物质的饱和溶液降温到60℃,其中溶质质量分数不变的物质是C.
(3)精制A时,通常采用的是蒸发溶剂的方法而不用降低溶液温度的方法,请据表分析,其原因是A的溶解度受温度影响不大.
(4)20℃时,溶解3.5g的固体C,蒸馏水的最佳使用量约为10ml.
17.分类、类比是学习化学常用的方法.
(1)金属资源储量有限,保扩金属资源是毎一个公民的义务.下面是一些常见的保护金属资源的事例:
①把某些金属制成合金 ②给自行车的链条涂油 ③用汽车用过的铅酸蓄电池再生铅
④铁制品表面镀上铬、镍等金属 ⑤用废电池的锌皮做制取氢气的实验
⑥将铝制品易拉罐置于“可回收”的垃圾桶内
请从保护金属资源有效途径的角度,将上述事例平均为两分类:
其中的一个分类标准是防止金属腐蚀;包括事例为①②④(填序号)
(2)在初中,我们已经学习过几种典型的酸,到了高中我们会学习到更多种类的酸:
观察表格,经过分析和类比回答:
①硫酸和高氯酸中,酸性相对更强的是高氯酸;
②高氯酸和氢氧化钡溶液反应,无明显现象.此反应的化学方程式为Ba(OH)2+2HClO4═Ba(ClO4)2+2H2O.
(1)金属资源储量有限,保扩金属资源是毎一个公民的义务.下面是一些常见的保护金属资源的事例:
①把某些金属制成合金 ②给自行车的链条涂油 ③用汽车用过的铅酸蓄电池再生铅
④铁制品表面镀上铬、镍等金属 ⑤用废电池的锌皮做制取氢气的实验
⑥将铝制品易拉罐置于“可回收”的垃圾桶内
请从保护金属资源有效途径的角度,将上述事例平均为两分类:
其中的一个分类标准是防止金属腐蚀;包括事例为①②④(填序号)
(2)在初中,我们已经学习过几种典型的酸,到了高中我们会学习到更多种类的酸:
| 非金属元素 | Si | P | S | Cl | |
| 最高价含氧酸 | 名称 | (偏)硅酸 | 磷酸 | 硫酸 | 高氯酸 |
| 化学式 | H2SiO3 | H3PO4 | H2SO4 | HClO4 | |
| 酸性 | 弱 | 中强 | 强 | 强 | |
①硫酸和高氯酸中,酸性相对更强的是高氯酸;
②高氯酸和氢氧化钡溶液反应,无明显现象.此反应的化学方程式为Ba(OH)2+2HClO4═Ba(ClO4)2+2H2O.
14.下列关系中,正确的是( )
| A. | pH:酸雨>正常雨水 | |
| B. | 常温条件下在水中的溶解性:氢氧化钙>氢氧化钠 | |
| C. | 溶于水后溶液的温度:氢氧化钠>硝酸铵 | |
| D. | 所有原子中:质子数>核外电子数 |
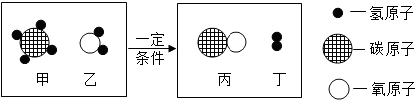
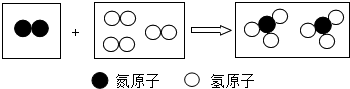 如图是某反应的微观过程.
如图是某反应的微观过程.