题目内容
6.下列说法正确的是( )| A. | K2MnO4、KMnO4、MnO2三者中Mn元素的化合价逐渐升高 | |
| B. | FeO、Fe2O3、Fe3O4 三者含氧的质量分数逐渐增大 | |
| C. | NH4NO3、NaCl、CaO三者溶于水后,所得溶液的温度逐渐升高 | |
| D. | NaCl、Na2CO3、NaOH三者饱和溶液的pH逐渐变大 |
分析 A、根据在化合物中正负化合价代数和为零进行分析;
B、如果直接计算,那么计算量会非常的大,这三种物质都是由铁元素和氧元素组成的,故我们可以通过原子个数比来解决;
C、根据物质溶于水溶液的温度变化情况分析;
D、根据NaCl、Na2CO3、NaOH三者饱和溶液的pH分析.
解答 解:A、根据在化合物中正负化合价代数和为零,KMnO4中Mn元素的化合价为:(+1)+a+(-2)×4,则a=+7;K2MnO4中Mn元素的化合价为:(+1)×2+b(-2)×4=0,则b=+6;MnO2中Mn元素的化合价为:c+(-2)×2=0,则c=+4;故错误;
B、FeO中铁原子和氧原子的个数比为:Fe:O═1:1;Fe2O3中铁原子和氧原子的个数比为:Fe:O═2:3;Fe3O4中铁原子和氧原子的个数比为:Fe:O═3:4;原子个数比值最高的其中含铁元素的质量分数也就是最高的,故错误;
C、NH4NO3溶于水温度降低,NaCl溶于水溶液温度不变,CaO溶于水与水反应放热,温度升高,三者溶于水后,所得溶液的温度逐渐升高,故正确;
D、NaCl、Na2CO3、NaOH三者饱和溶液的pH分别是7、大于7、大于7,其中后两者由于没有指明温度,因此pH无法判断,故错误.
故选C.
点评 本题难度不大,掌握元素化合价的计算方法、元素的质量分数、物质溶于水后温度变化情况以及溶液的pH值等是解决此题的关键.

练习册系列答案
相关题目
17.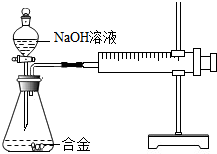 合金在生活中应用十分广泛.已知某合金粉末除含铝外,还含有铁、铜中的一种或两种.小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动.
合金在生活中应用十分广泛.已知某合金粉末除含铝外,还含有铁、铜中的一种或两种.小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动.
【提出问题】难道NaOH溶液也能与某些金属发生化学反应吗?
【查阅资料】
(1)铝能与氢氧化钠溶液反应,铁、铜不能与氢氧化钠溶液反应.
(2)铝与氢氧化钠溶液反应的化学方程式为:2AI+2NaOH+2H2O═2NaAIO2+3H2↑
(NaAlO2溶于水,溶液显无色)
进行猜想】猜想1:该合金粉末中除铝外,还含有铁
猜想2:该合金粉末中除铝外,还含有铜
猜想3:该合金粉末中除铝外,还含有铁、铜.
实验探究】下列实验(见表1)仅供选用的试剂:20%的硫酸溶液、30%的NaOH溶液.
表1实验记录
【得出结论】猜想3成立.
【反思】
1.一般来说,活泼金属能与稀硫酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.铝与稀硫酸发生化学反应的化学方程式是2Al+3H2SO4═Al2(SO4)3+3H2↑
2.上述实验中用到的稀硫酸由浓硫酸稀释得到,稀释浓硫酸的方法是:把浓硫酸沿烧杯壁慢慢注入水中,并不断搅拌.
3.若小明向合金粉末中加入的是足量的稀硫酸,则最终剩余的固体成分是铜.
拓展与分析】为了比较铝、铁、铜的金属活动性强弱,某同学设计一个实验方案,将金属铝和铜插入到硫酸亚铁溶液中其现象是铝表面有一层红色物质出现,铜表面无现象.,说明铝、铁、铜金属活动性由弱到强顺序是铝>铁>铜.
 合金在生活中应用十分广泛.已知某合金粉末除含铝外,还含有铁、铜中的一种或两种.小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动.
合金在生活中应用十分广泛.已知某合金粉末除含铝外,还含有铁、铜中的一种或两种.小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动.【提出问题】难道NaOH溶液也能与某些金属发生化学反应吗?
【查阅资料】
(1)铝能与氢氧化钠溶液反应,铁、铜不能与氢氧化钠溶液反应.
(2)铝与氢氧化钠溶液反应的化学方程式为:2AI+2NaOH+2H2O═2NaAIO2+3H2↑
(NaAlO2溶于水,溶液显无色)
进行猜想】猜想1:该合金粉末中除铝外,还含有铁
猜想2:该合金粉末中除铝外,还含有铜
猜想3:该合金粉末中除铝外,还含有铁、铜.
实验探究】下列实验(见表1)仅供选用的试剂:20%的硫酸溶液、30%的NaOH溶液.
表1实验记录
| 实验步骤 | 实验现象 | 结论 |
| ①取一定量的合金粉末,加过量的30%氢氧化钠溶液,充分反应后过滤,滤渣备用 | 粉末部分溶解,并有无色气体放出 | 合金中一定含有铝 |
| ②取步骤①所得滤渣,加过量20%的硫酸溶液,充分反应 | 滤渣部分溶解,并有无色气体放出,溶液呈浅绿色 | 合金中一定含有铁、铜 |
【反思】
1.一般来说,活泼金属能与稀硫酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.铝与稀硫酸发生化学反应的化学方程式是2Al+3H2SO4═Al2(SO4)3+3H2↑
2.上述实验中用到的稀硫酸由浓硫酸稀释得到,稀释浓硫酸的方法是:把浓硫酸沿烧杯壁慢慢注入水中,并不断搅拌.
3.若小明向合金粉末中加入的是足量的稀硫酸,则最终剩余的固体成分是铜.
拓展与分析】为了比较铝、铁、铜的金属活动性强弱,某同学设计一个实验方案,将金属铝和铜插入到硫酸亚铁溶液中其现象是铝表面有一层红色物质出现,铜表面无现象.,说明铝、铁、铜金属活动性由弱到强顺序是铝>铁>铜.
1.研究性学习小组测定实验室里一瓶久置的NaOH固体是否变质.
【提出问题】NaOH固体是否变质?
【猜想与假设】猜想1:没变质,全部是NaOH;
猜想2:全变质,全部是Na2CO3
猜想3:部分变质,既含有NaOH,又含有Na2CO3;
设计方案并进行实验】请你与他们一起完成,并回答所给问题.
上述步骤①中,滴加过量氯化钙溶液的目的是使样品中的Na2C03完全反应
【实验结论】通过实验,说明上述猜想中3是正确的.
【拓展】
要除去氢氧化钠中含有的碳酸钠,所用的方法(用化学方程式表示)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
【反思】通过探究,实验室中的氢氧化钠应密封保存.
【提出问题】NaOH固体是否变质?
【猜想与假设】猜想1:没变质,全部是NaOH;
猜想2:全变质,全部是Na2CO3
猜想3:部分变质,既含有NaOH,又含有Na2CO3;
设计方案并进行实验】请你与他们一起完成,并回答所给问题.
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述固体样品8g溶于100mL水配成溶液,向溶液中滴加 过量的氯化钙溶液充分反应后,静置. | 产生白色沉淀 | 说明久置固体中,一定含有Na2CO3 |
| ②用玻璃棒蘸取少量①中的上层清液滴在pH试纸上,与标准比色卡对比,测出pH | pH=10 | 说明固体中,还一定含有NaOH(填化学式). |
【实验结论】通过实验,说明上述猜想中3是正确的.
【拓展】
要除去氢氧化钠中含有的碳酸钠,所用的方法(用化学方程式表示)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
【反思】通过探究,实验室中的氢氧化钠应密封保存.
18.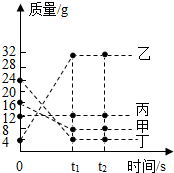 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示.下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示.下列说法中不正确的是( )
 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示.下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示.下列说法中不正确的是( )| A. | 乙物质一定是化合物 | |
| B. | 丙可能为该反应的催化剂 | |
| C. | 该反应中,乙、丁的质量变化之比为7:5 | |
| D. | 该反应中,甲、乙的质量变化之比为1:4 |
15.下列食品或调味品的制作过程中,没有新物质生成的是( )
| A. | 粮食酿白酒 | B. | 用水果榨成果汁 | ||
| C. | 牛奶变酸奶 | D. | 用小苏打焙制糕点 |
19.下列物质,不能用金属和酸反应直接制得的是( )
| A. | ZnCl2 | B. | CuCl2 | C. | FeCl2 | D. | FeSO4 |