题目内容
9.读图,回答下列问题: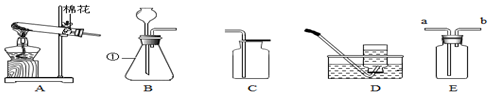
(1)写出标号①的仪器名称锥形瓶
(2)用A装置制取氧气时,反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑用D装置收集氧气,当气泡连续均匀冒出时开始收集
(3)用A、D装置制取氧气,实验结束时,应先将导管移出水面(将导管移出水面或熄灭酒精灯)
(4)用B、E、C装置制取并收集干燥的二氧化碳,E中盛放的试剂是浓硫酸.验证C装置已收集满二氧化碳的方法是将燃着的木条放在集气瓶口,火焰熄灭,则二氧化碳收集满.加试剂前,连接装置并检查装置的气密性.将二氧化碳通入盛有蒸馏水的试管中,该试管中溶液的PH<7
(5)氨气(NH3)是一种无色有刺激性气味,极易溶于水的气体.实验室常用氯化铵晶体和氢氧化钙粉末混合加热来制取氨气,同时生成氯化钙和水,写出制取氨气的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;选取上述A(填字母)作为制取氨气的发生装置,收集氨气选用的装置为E(填字母)
分析 (1)熟悉常见仪器,根据仪器的形状和用途判断名称;
(2)根据发生装置的特点可判断反应物状态和反应条件;根据收集装置可判断气体的性质,综合后可判断制取的气体;
(3)根据排水法收集氧气时的注意事项解答;
(4)实验室用大理石与稀盐酸制取二氧化碳,制取的二氧化碳中含有少量的水蒸气去分析解答;
(5)根据实验室常用氯化铵晶体和氢氧化钙粉末混合加热来制取氨气,因此需要加热;氯化铵和氢氧化钙在加热的条件下生成氯化钙和氨气和水,配平即可;氨气是一种密度比空气小、极易溶于水的气体,因此氨气只能用向下排空气法收集解答;
解答 解:
(1)实验仪器a的名称是锥形瓶;
(2)图中试管内有棉花,应用高锰酸钾制氧气,高锰酸钾在加热的条件下,生成锰酸钾和二氧化锰和氧气,反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2 MnO4+MnO2+O2↑;当观察到D装置中气泡连续均匀放出时,开始收集氧气.
(3)用A、D装置制取氧气,实验结束时,为防止冷凝水倒流入试管,应先将导管移出水面,再熄灭酒精灯;
(4)实验室用B、E、C装置制取并收集干燥的二氧化碳,浓硫酸具有吸水性,可做干燥剂;故E中应盛放的试剂是浓硫酸;验证C装置已收集满二氧化碳的方法是:将燃着的木条放在集气瓶口,火焰熄灭,则二氧化碳收集满;加试剂前,连接装置并检查装置的气密性;将二氧化碳通入盛有蒸馏水的试管中,二氧化碳与水反应,生成碳酸,该试管中溶液的pH<7;
(5)实验室常用氯化铵晶体和氢氧化钙粉末混合加热来制取氨气,因此需要加热;氯化铵和氢氧化钙在加热的条件下生成氯化钙和氨气和水,化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;氨气是一种密度比空气小、极易溶于水的气体,因此氨气只能用向下排空气法收集.
答案:
(1)锥形瓶;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;气泡连续均匀冒出;
(3)将导管移出水面;
(4)浓硫酸; 将燃着的木条放在集气瓶口,火焰熄灭,则二氧化碳收集满.气密性、<;
(5)2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O、A、E
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| 序号 | ① | ② | ③ | ④ | ⑤ |
| 物质名称 | 甲烷 | 氧气 | 烧碱 | 干冰 | 五氧化二磷 |
| 化学式 | CH4 | O2 | NaOH | CO2 | P2O5 |
(2)表中的物质可用于人工降雨的是④,可用于制肥皂、造纸等工业的碱是③.
(3)若要测定某烧碱溶液的酸碱度,不能选用下列选项中的①②.
①无色酚酞溶液; ②紫色石蕊溶液; ③pH试纸
(4)我国福建生产一种槟榔芋,芋皮上含有一种碱性的物质--皂角素,皮肤沾上它会奇痒难忍.你认为可选用下列中的①④来涂抹止痒.
①食醋; ②熟石灰; ③肥皂水; ④柠檬汁.
| A. |  测溶液的pH | B. |  检查装置的气密性 | ||
| C. |  点燃酒精灯 | D. |  加热试管中液体 |
【查阅资料】铁的活动性比铜强.
【进行猜想】对三种金属的活动性顺序做出如下猜想:
猜想一:R>Fe>Cu; 猜想二:Fe>R>Cu; 猜想三:Fe>Cu>R
【收集证据】为了验证哪一种猜想成立,甲、乙、丙三位同学分别展开实验探究.
| 主要操作 | 主要现象 | 实验结论 | |
| 甲 | 将打磨好的R丝插入盛有硫酸铜溶液的试管中 | R丝表面附着一层红色固体 | 猜想一 正确 |
| 乙 | 将粗细相同打磨好的R丝、铁丝,分别插入体积和溶质质量分数都相同的稀盐酸中 | R丝表面产生气泡速率比铁丝表面产生气泡速率快(填“快”或“慢”) | |
| 丙 | 将粗细相同打磨好的R丝、铁丝,分别在空气中点燃 | R丝在空气中剧烈燃烧,铁丝在 空气中不能燃烧 |
【交流反思】三位同学交流讨论后认为,比较金属活动性强弱的方法有多种.
【归纳总结】他们总结得出比较金属活动性强弱的常见方法有:
(1)金属与氧气反应的难易和剧烈程度;
(2)金属与酸溶液是否反应或反应的剧烈程度;
(3)金属与盐溶液是否反应.

 稀盐酸与氢氧化钠溶液反应时溶液的PH变化如图所示.请回答下列问题:
稀盐酸与氢氧化钠溶液反应时溶液的PH变化如图所示.请回答下列问题: 石灰石与一定量的稀盐酸反应后的溶液pH为2,现向适量该溶液中逐滴加入碳酸钠溶液,请你画溶液pH随加入碳酸钠溶液的量的变化曲线,并说明理由.
石灰石与一定量的稀盐酸反应后的溶液pH为2,现向适量该溶液中逐滴加入碳酸钠溶液,请你画溶液pH随加入碳酸钠溶液的量的变化曲线,并说明理由.