题目内容
18. 石灰石与一定量的稀盐酸反应后的溶液pH为2,现向适量该溶液中逐滴加入碳酸钠溶液,请你画溶液pH随加入碳酸钠溶液的量的变化曲线,并说明理由.
石灰石与一定量的稀盐酸反应后的溶液pH为2,现向适量该溶液中逐滴加入碳酸钠溶液,请你画溶液pH随加入碳酸钠溶液的量的变化曲线,并说明理由.
分析 根据向盐酸和氯化钙的混合溶液逐渐滴加碳酸钠,碳酸钠会先与盐酸反应,溶液的pH值从2逐渐增大到7,然后碳酸钠和与氯化钙反应,溶液的pH值不变,氯化钙完全反应后,继续滴加碳酸钠,溶液的pH值逐渐增大进行分析.
解答 解:向盐酸和氯化钙的混合溶液逐渐滴加碳酸钠,碳酸钠会先与盐酸反应,溶液的pH值从2逐渐增大到7,然后碳酸钠和与氯化钙反应,溶液的pH值不变,氯化钙完全反应后,继续滴加碳酸钠,溶液的pH值逐渐增大,所以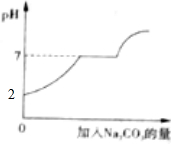
故答案为:
碳酸钠会先与盐酸反应,溶液的pH值从2逐渐增大到7,然后碳酸钠和与氯化钙反应,溶液的pH值不变,氯化钙完全反应后,继续滴加碳酸钠,溶液的pH值逐渐增大.
点评 本题是借助于数学模型,利用图象的方式来分析和解决有关问题,要结合发生的化学反应正确分析图象与反应的关系.

练习册系列答案
相关题目
8.下列解释中不正确的是( )
| A. | 将气体压缩到钢瓶中--分子间有间隙,且气体分子间的间隙大 | |
| B. | 液态氧和氧气都能支持燃烧--同种物质的分子化学性质相同 | |
| C. | 缉毒犬能根据气味发现毒品--分子在不断运动 | |
| D. | 变瘪的乒乓球放入热水中能鼓起来--分子受热体积变大 |
6.《美国化学会志》报道了中国科学家以二氧化碳和钠在一定条件制得金刚石,其化学方程式为3CO2+4Na=2X+C(金刚石).则X的化学式为( )
| A. | Na2CO3 | B. | Na2O2 | C. | Na2O | D. | Na4C2O6 |
13.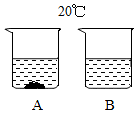 分析处理图表中的信息是学习科学的一种基本技能.如表是氯化钠在不同温度时的溶解度,根据此表回答:
分析处理图表中的信息是学习科学的一种基本技能.如表是氯化钠在不同温度时的溶解度,根据此表回答:
(1)在20℃时,A、B两个烧杯装了100克水,分别取30克和40克氯化钠溶于烧杯中,充分溶解后如图所示,则一定是饱和溶液的是B(填字母).图B中所得溶液的质量是136克.
(2)若要从氯化钠溶液中结晶获得氯化钠晶体,应采用什么方法?蒸发结晶.
 分析处理图表中的信息是学习科学的一种基本技能.如表是氯化钠在不同温度时的溶解度,根据此表回答:
分析处理图表中的信息是学习科学的一种基本技能.如表是氯化钠在不同温度时的溶解度,根据此表回答:| 温度/℃ | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
(2)若要从氯化钠溶液中结晶获得氯化钠晶体,应采用什么方法?蒸发结晶.
3.生活中处处有化学.下列说法合理的是( )
| A. | 用肥皂水涂在蚊虫叮咬处止痒 | |
| B. | 焚烧废旧塑料解决白色污染 | |
| C. | 硒有抗癌作用,需大量补充 | |
| D. | 农药、化肥施用后会残留在农产品上,应禁止施用 |
10.下列实验方案能达到实验目的是A.
| 选项 | 实验目的 | 实验方案 |
| A | 区分纯羊毛织品和涤纶织品 | 取样灼烧后闻气味 |
| B | 证明温度越高分子运动越快 | 把一滴蓝墨水滴入一杯纯净水中 |
| C | 探究铜、银的金属活动性 | 将打磨好的铜、银片分别插入稀硫酸中 |
| D | 除去CO2中少量的CO | 通过灼热的氧化铜 |
7.请根据下列实验回答问题:
溶液②的质量为131.6g,属于不饱和溶液的是①(填序号)
| 实验操作 | 实验结果 |
| 取100ml水,加入25g硝酸钾,搅拌 | 全部溶解,得溶液① |
| 再加10g硝酸钾,搅拌,还有3.4g固体不溶 | 得溶液② |
8.下列是几种粒子的结构示意图,其中属于阴离子的是( )
| A. | 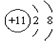 | B. | 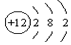 | C. |  | D. | 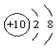 |