题目内容
4. 稀盐酸与氢氧化钠溶液反应时溶液的PH变化如图所示.请回答下列问题:
稀盐酸与氢氧化钠溶液反应时溶液的PH变化如图所示.请回答下列问题:(1)从pH的变化图线来看,该操作是把氢氧化钠溶液逐滴加入到稀盐酸中;
(2)表示两种溶液恰好完全反应的点是n(填m、n或p);
(3)P点时的溶液中,溶质是NaCl、NaOH(写化学式),滴入石蕊后溶液呈现蓝色.
分析 (1)根据pH值的图象的变化趋势进行分析.
(2)根据两种溶液恰好完全反应时溶液的pH等于7分析.
(3)根据P点表示氢氧化钠溶液过量分析.
解答 解:(1)根据pH值的图象的变化趋势可以看出,pH值是由小于7逐渐增大到7再大于7,可以得出原溶液是酸性的,因此该操作是把氢氧化钠溶液逐滴加入到稀盐酸中.
(2)两种溶液恰好完全反应时溶液的pH等于7,因此两种溶液恰好完全反应的点是n.
(3)P点表示氢氧化钠溶液过量,因此P点时的溶液中,溶质是生成的氯化钠和过量的氢氧化钠,溶液显碱性,滴入石蕊后溶液呈现蓝色.
故填:(1)氢氧化钠溶液;稀盐酸;(2)n;(3)NaCl、NaOH;蓝.
点评 本题主要考查了根据图象对中和反应的正确的判断和理解,难度不大,综合性强.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.下列关于碳和一氧化碳的叙述中,正确的是( )
| A. | 都能跟氧化铜发生置换反应,具有还原性 | |
| B. | 常温下都是气体 | |
| C. | 都能在空气中燃烧,都可以作燃料 | |
| D. | 都有毒性 |
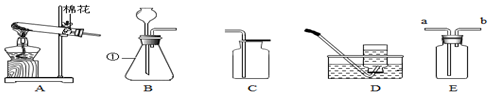
15.规范的操作是试验成功的保证,下列实验操作正确的是( )
| A. |  验满氧气 | B. |  量取液体读数 | ||
| C. |  过滤 | D. |  检查装置气密性 |
12.下列关于O2、CO2、SO2的说法正确的是( )
| A. | 都含有氧元素 | B. | 都含有氧分子 | C. | 都含有氧气 | D. | 都含有氧离子 |
19.下表列出了部分元素的原子结构示意图,请回答下列问题:
(1)氯化镁的构成粒子是镁离子和氯离子.
(2)氯原子在化学反应中易得到(填“得到”或“失去”)电子;带有1个单位负电荷,成为阴离子.
(3)从上图中可以知道Al3+与氧原子具有相同的电子层数.
| 元素 | O | Mg | Al | Cl |
| 原子结构 示意图 |  | 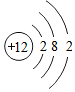 | 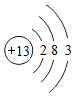 | 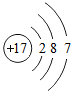 |
(2)氯原子在化学反应中易得到(填“得到”或“失去”)电子;带有1个单位负电荷,成为阴离子.
(3)从上图中可以知道Al3+与氧原子具有相同的电子层数.
16.下列除杂(括号内为杂质)的实验过程都正确的是( )
| A. | KCl(K2CO3)加足量稀盐酸、过滤、蒸发、结晶 | |
| B. | MnO2 (KCl)加水溶解、过滤、蒸发、结晶 | |
| C. | CuO(Cu)加足量稀盐酸、过滤、洗涤、干燥 | |
| D. | BaSO4(BaCO3)加足量稀盐酸、过滤、洗涤、干燥 |
13. 分析处理图表中的信息是学习科学的一种基本技能.如表是氯化钠在不同温度时的溶解度,根据此表回答:
分析处理图表中的信息是学习科学的一种基本技能.如表是氯化钠在不同温度时的溶解度,根据此表回答:
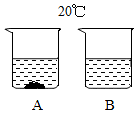
(1)在20℃时,A、B两个烧杯装了100克水,分别取30克和40克氯化钠溶于烧杯中,充分溶解后如图所示,则一定是饱和溶液的是B(填字母).图B中所得溶液的质量是136克.
(2)若要从氯化钠溶液中结晶获得氯化钠晶体,应采用什么方法?蒸发结晶.
 分析处理图表中的信息是学习科学的一种基本技能.如表是氯化钠在不同温度时的溶解度,根据此表回答:
分析处理图表中的信息是学习科学的一种基本技能.如表是氯化钠在不同温度时的溶解度,根据此表回答:| 温度/℃ | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
(2)若要从氯化钠溶液中结晶获得氯化钠晶体,应采用什么方法?蒸发结晶.