题目内容
12.将锌粉、铝粉、铁粉、和镁粉混合物159g与一定质量浓度为35%的硫酸溶液恰好完全反应,蒸干水分得固体(不含结晶水)639g,反应中产生H2质量可能为( )| A. | 10g | B. | 49g | C. | 159g | D. | 480g |
分析 根据质量守恒定律可知,反应物的质量之和等于生成物的质量之和,反应前后元素的种类,原子的数目均不变.
解答 解:根据题目信息可知,混合物和硫酸恰好完全反应,因此混合物和纯硫酸(H2SO4)的质量之和等于剩余固体和氢气的质量之和.反应前后硫酸根的质量=(639克-159克)=480克,则硫酸的质量=480克÷$\frac{96}{98}$=490克.因此氢气的质量=硫酸中的氢元素的质量=490克-480克=10克.
故选A.
点评 本题的关键是先计算出硫酸根的质量,然后算出纯硫酸的质量;注意质量守恒定律中的质量指的是参加反应的质量,因此代入的数据是纯硫酸的质量,而不是硫酸溶液的质量.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
7.铜与浓硫酸发生的反应为:Cu+2H2SO4(浓)═CuSO4+SO2↑+2H20.有关CuSO4制备途径及性质如图所示,下列说法错误的是( )


| A. | 反应①②中均有一种元素的化合价发生变化 | |
| B. | 反应③和④中的铜元素质量未发生改变 | |
| C. | 途径②比途径①更好地体现了绿色化学思想 | |
| D. | 反应④说明某些碱受热分解生成金属氧化物 |
17.在硝酸银、硝酸铜和硝酸锌的混合溶液中,加入一定量的铁粉,反应后过滤,则滤液中一定含( )
| A. | Ag+、Cu2+、Zn2+ | B. | Ag+、Cu2+、Zn2+、Fe2+ | ||
| C. | Cu2+、Zn2+ | D. | Zn2+、Fe2+ |
1.为了分析某食盐水中NaCl的含量,甲、乙、丙三位同学利用NaCl和AgNO3溶液发生反应生成AgCl沉淀的方法分别进行了实验,他们的实验数据如下表:
(1)NaCl和AgNO3溶液反应的化学方程式为NaCl+AgNO3=AgCl↓+NaNO3.
(2)列出求解参加反应的硝酸银质量(x)的比例式$\frac{170}{x}$=$\frac{143.5}{1.435g}$.
(3)丙同学实验后溶液中溶质的组成有NaNO3、AgNO3.
(4)恰好完全反应那次实验结束后所得溶液中再加入1.435g水后所得溶液的溶质质量分数为0.85%.
| 甲 | 乙 | 丙 | |
| 所取食盐水的质量/g | 100 | 50 | 50 |
| 加入AgNO3溶液的质量/g | 50 | 50 | 75 |
| 反应后所得沉淀物的质量/g | 1.435 | 1.435 | 1.435 |
(2)列出求解参加反应的硝酸银质量(x)的比例式$\frac{170}{x}$=$\frac{143.5}{1.435g}$.
(3)丙同学实验后溶液中溶质的组成有NaNO3、AgNO3.
(4)恰好完全反应那次实验结束后所得溶液中再加入1.435g水后所得溶液的溶质质量分数为0.85%.



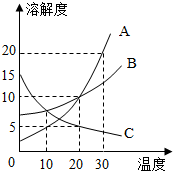 如图A、B、C三种固体物质的溶解度曲线.请回答以下问题:
如图A、B、C三种固体物质的溶解度曲线.请回答以下问题: