题目内容
14.用加热高锰酸钾的方法制取氧气.(2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑)(1)算出高锰酸钾(KMnO4)中各元素的质量比,即:K:Mn:O=39:55:64
(2)要得到3.2g的氧气,至少需要高锰酸钾的质量是多少?
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据高锰酸钾受热分解的化学方程式,可得知反应中高锰酸钾与氧气的质量关系,再由生成氧气的质量即可计算所需要高锰酸钾的质量.
解答 解:(1)高锰酸钾中组成各元素的质量比K:Mn:O=39:55:(16×4)=39:55:64.
故答案为:(1)39:55:64;
(2)设需高锰酸钾的质量为x
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
x 3.2g
$\frac{316}{x}=\frac{32}{3.2g}$
x=31.6g
所以需要高锰酸钾的质量是31.6g.
故答案为:需要高锰酸钾的质量是31.6g.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算、根据化学方程式计算类问题中的基础计算,以及进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列有关溶液的说法,正确的是( )
| A. | 均一、稳定的液体都是溶液 | |
| B. | 正常雨水的pH<7,是因为H2O+CO2═H2CO3 | |
| C. | 如右图,50℃时,把30 g甲放入50 g水中能形成80 g甲的饱和溶液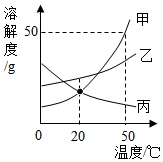 | |
| D. | 氯化钠的溶解度随温度的变化不明显,从氯化钠溶液中得到氯化钠固体可采用冷却热饱和溶液的方法 |
2.现有三个集气瓶,分别盛有氧气、空气和二氧化碳三种无色气体,能把这三瓶气体区别开的方法是( )
| A. | 往三个集气瓶中分别倒入少量石灰水并振荡 | |
| B. | 燃着的木条分别伸入三集气瓶中 | |
| C. | 用带火星的木条分别放到三个集气瓶瓶口 | |
| D. | 以上三种方法都可以 |
19.下列有关化学方程式的书写正确的是( )
| A. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | B. | S+O2↑$\frac{\underline{\;点燃\;}}{\;}$SO2 | ||
| C. | H2O═H2↑+O2↑ | D. | 2NaOH+CuSO4═Cu(OH)2↓+Na2SO4 |