题目内容
5.野炊过程实际上是运用化学知识分析、解决问题的过程.某次野炊活动中,同学们携带了铁锅、牛肉、面条、西红柿、食用油、食盐、味精、食醋以及去污粉(去污粉的有效成份为碳酸钠)和“84消毒液”等物品.(1)携带过程中,不慎将装食盐、去污粉的瓶子混淆了.若要将它们区分开来,适宜选食醋(填携带的物品名称).
(2)新购置的餐具常常用少量“84消毒液”来浸泡进行杀菌消毒.制备“84消毒液”的主要反应为:2NaOH+Cl2=NaClO+NaCl+H2O.若要证明“84消毒液”中含有NaCl,其方法是:取少量“84消毒液”,加入少量某种溶液后,观察到产生不溶于稀硝酸的白色沉淀,其反应的化学方程式为NaCl+AgNO3=AgCl↓+NaNO3.
(3)野炊结束时,小辉用干布抹去铁锅表面的水珠.这样做的目的是防止铁锅生锈.
分析 (1)根据碳酸盐会与酸反应生成二氧化碳,氯化钠不会与酸反应进行分析;
(2)根据氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠进行分析;
(3)根据铁生锈的条件进行分析.
解答 解:(1)食盐是NaCl,去污粉的主要成份是Na2CO3,而食醋中的醋酸(CH3COOH)可与碳酸钠发生反应生成气体,与NaCl不反应,可以鉴别,把两者区分开来;
(2)氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠,化学方程式为:NaCl+AgNO3=AgCl↓+NaNO3;
(3)铁在潮湿空气中会生锈,因此要防铁锅生锈,需保持其干燥.
故答案为:(1)食醋;
(2)NaCl+AgNO3=AgCl↓+NaNO3;
(3)防止铁锅生锈.
点评 本题考查了化学知识在生活中的应用,可让学生体验到所学可为所用,学之乐趣无穷.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.现有一不纯的氧化铜样品16g可能混有氧化铁、氧化镁、木炭粉、氯化钠中的一种或几种,加入200g稀硫酸恰好完全反应,没有固体剩余,生成3.6g水,则下列判断正确的是( )
| A. | 原固体样品中肯定含有木炭粉 | |
| B. | 原固体样品中只混有氧化镁 | |
| C. | 恰好完全反应后溶液中水的质量为184克 | |
| D. | 所用的稀硫酸中溶质质量分数为19.6% |
20.已知MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2X+Cl2↑,则X的化学式为( )
| A. | H2 | B. | O2 | C. | H2O | D. | H2O2 |
14.锶元素的粒子结构示意图和在元素周期表中显示的信息如图所示,下列说法错误的是( )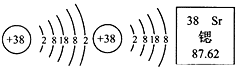

| A. | 锶的相对原子质量为87.62g | B. | 锶原子核外共有38个电子 | ||
| C. | 锶元素属于金属元素 | D. | 硫酸锶的化学式可表示为SrSO4 |
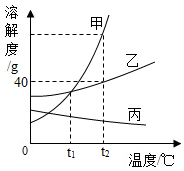 如图是甲、乙、丙三种固体的溶解度曲线,回答下列问题
如图是甲、乙、丙三种固体的溶解度曲线,回答下列问题

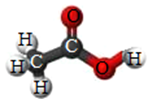 如图为某分子的结构模型,请回答下列问题:
如图为某分子的结构模型,请回答下列问题: