题目内容
16.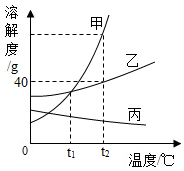 如图是甲、乙、丙三种固体的溶解度曲线,回答下列问题
如图是甲、乙、丙三种固体的溶解度曲线,回答下列问题(1)t1℃时,甲的溶解度>丙的溶解度(填“>”、“<”或“=”)
(2)t2℃时,向50克水中加入50g乙物质,充分溶解后所得溶液的质量是70g.
(3)t1℃甲、乙、丙的饱和溶液升温到t2℃,所得溶液中溶质质量分数的大小关系为甲=乙>丙(填“>”、“<”或“=”).
(4)用同一种方法可以使甲、乙、丙三种物质的溶液都有晶体析出,该方法是蒸发结晶.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,t1℃时,甲的溶解度>丙的溶解度;
(2)t2℃时,乙物质的溶解度是40g,所以向50克水中加入50g乙物质,充分溶解后所得溶液的质量是70g;
(3)t1℃时,甲、乙物质的溶解度相等,大于丙物质的溶解度,升高温度不会析出晶体,丙物质会析出晶体,所以t1℃时,甲、乙、丙的饱和溶液升温到t2℃,所得溶液中溶质质量分数的大小关系为:甲=乙>丙;
(4)甲、乙物质的溶解度随温度的升高而增大,乙物质的溶解度随温度的升高而减小,所以用同一种方法可以使甲、乙、丙三种物质的溶液都有晶体析出,该方法是蒸发结晶.
故答案为:(1)>;
(2)70g;
(3)甲=乙>丙;
(4)蒸发结晶.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
13.下列各组物质中按酸、碱、盐、单质的顺序排列正确的是( )
| A. | 硫酸、氧化钠、氯化钙、金刚石 | B. | 碳酸氢钠、氢氧化钡、氯化钠、锌 | ||
| C. | 硝酸、氢氧化钾、纯碱、氧气 | D. | 盐酸、苛性钠、纯碱、二氧化硅 |
4.规范的操作是实验成功的保证.下列实验操作正确的是( )
| A. | 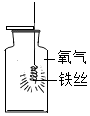 铁在氧气中燃烧 | B. | 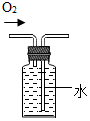 收集氧气 | C. | 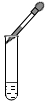 滴加液体 | D. | 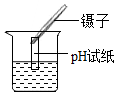 测溶液的pH值 |
11.已知M、N在一定条件下,能发生反应:xM+yN=mP+nQ,则下列说法中正确的是( )
| A. | 化学计量数x与y的和一定等于m与n的和 | |
| B. | M、N、P、Q中可能含有同一种元素 | |
| C. | 若M、N为单质和化合物,则该反应一定是置换反应 | |
| D. | 反应物M、N中所含元素种类与生成物P、Q中所含元素种类不一定相同 |