题目内容
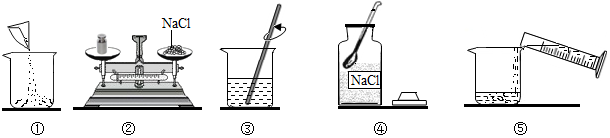
2.分析下面两个基础实验,回答问题:【实验一】(1)粗盐中含有泥沙等不溶性杂质.粗盐提纯的操作步骤如图1所示.

溶解粗盐过程中,搅拌的作用是加快溶解的速率.
(2)在过滤操作中,玻璃棒的作用是引流.
(3)如果过滤后的滤液仍较浑浊,可能的原因有BC(填标号).
A.过滤器内滤纸的高度低于漏斗边缘
B.倾倒液体时,液面超过滤纸的高度
C.实验中滤纸被划破
(4)在蒸发操作中,待蒸发皿中出现较多(填“较多”或“较少”)量固体时,应停止加热.
【实验二】配制50g一定溶质质量分数的氯化钠溶液,实验步骤如下:
(1)计算:氯化钠质量和水的体积.(水的密度:1.0g/mL)
(2)称量:如图2所示(右盘无砝码)称得的氯化钠质量为4g.
量取:选择量程为50(填“10”、“50”或“100”)mL的量筒准确量取46 mL水.
(3)溶解:把氯化钠和水全部转移到烧杯中,搅拌至氯化钠全部溶解.
(4)装瓶、贴标签:请填写图3所示标签.
【反思】(5)上述实验过程中,用量筒量取水时,若按图4方式进行读数,将导致所配制溶液的溶质质量分数偏小(填“偏大”、“不变”或“偏小”).
(6)若将上述50g氯化钠溶液稀释为2%的氯化钠溶液,稀释过程中,不需要用到的仪器有BD
A.量筒 B.漏斗 C.玻璃棒 D.托盘天平.
分析 【实验一】(1)根据溶解时玻璃棒搅拌能加速溶解速度进行分析;
(2)根据过滤时用玻璃棒引流液体进行分析;
(3)根据滤液不经过滤纸进入滤液就会造成滤液浑浊,A待过滤的物质经过过滤后进入滤液,BC有一部分待过滤的混合物不经过滤纸进入滤液造成滤液浑浊进行分析;
(4)根据蒸发不能蒸干要等到出现较多固体时停止加热进行分析;
【实验二】根据游码的示数是4g没用砝码确定质量,溶剂水的质量就是50g-4g=46g合46mL,选择和所需水的体积最接近且略大的量筒,然后根据溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%解答;标签上写明溶液的名称和溶质质量分数;
【反思】(5)仰视读数量取的水的体积偏大,所以配制的溶液溶质质量分数偏小;
(6)稀释只要计算出所需的水加水稀释即可,不需要漏斗和天平.
解答 解:【实验一】(1)溶解时玻璃棒搅拌能加速溶解速度;
(2)过滤时用玻璃棒引流液体;
(3)滤液不经过滤纸进入滤液就会造成滤液浑浊;
(4)蒸发不能蒸干要等到出现较多固体时停止加热;
【实验二】(2)根据游码的示数是4g没用砝码确定溶质质量4g;溶剂水的质量就是50g-4g=46g,合46mL,选择和所需水的体积最接近且略大的量筒;
(3)所配制的溶液的溶质质量分数=$\frac{4g}{50g}$×100%=8%;
(4)标签上写明溶液的名称和溶质质量分数;
【反思】(5)仰视读数量取的水的体积偏大,所以配制的溶液溶质质量分数偏小;
(6)稀释只要计算出所需的水加水稀释即可,不需要漏斗和天平,故选:BD.
故答案为:【实验一】(1)加快溶解的速率;
(2)引流;
(3)BC;
(4)较多;
【实验二】(2)4,50,46;
(4) ;
;
【反思】(5)偏小;
(6)BD.
点评 本题主要考查了粗盐的提纯和一定质量分数溶液的配制,难度不大,需要将题中的问题转化成学过的知识进行解答.

| A. | 水分子由氢元素与氧元素组成 | B. | 过滤可以降低水的硬度 | ||
| C. | 电解水时在负极得到氢气 | D. | 水由氢气和氧气组成 |
| A. | 二氧化碳由1个碳原子和2个氧原子构成 | |
| B. | 二氧化碳由碳氧两种元素组成 | |
| C. | 二氧化碳中碳元素和氧元素的质量比为3:8 | |
| D. | 等质量的二氧化碳和一氧化碳中所含碳元素质量比为7:11 |
| A. |  检验甲烷燃烧 | |
| B. |  读液体体积 | |
| C. |  将带有残留液有CO2生成的滴管倒持 | |
| D. |  吹灭酒精灯 |
| A. | 活性炭净水 | B. | 金刚石做钻头 | ||
| C. | 石墨制铅笔 | D. | 熟石灰改良酸性土壤 |
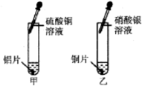
| A. | 胶头滴管的使用方法操作正确 | |
| B. | 该实验能得出金属活动性顺序为银>铜>铝 | |
| C. | 甲、乙中观察到的实验现象相同 | |
| D. | 甲、乙中发生的反应都属于置换反应 |
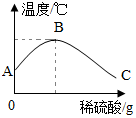 学习酸碱中和反应时,很多同学对其产生了探究兴趣.
学习酸碱中和反应时,很多同学对其产生了探究兴趣.