题目内容
2.化学兴趣小组的同学复习元素及其化合物知识以后,互相交流自己的学习体会,下面是四位同学的发言,你认为其中正确的是( )| A. | 浓盐酸、浓硫酸都能使纸张炭化 | |
| B. | CO、H2、O2、CH4均可作为燃料 | |
| C. | 烧碱溶液和石灰水都具有腐蚀性 | |
| D. | SO2、CO2、CO都可用氢氧化钠溶液吸收 |
分析 浓硫酸具有强氧化性,能够氧化纸张,而浓盐酸不具有强氧化性;
氧气不能燃烧;
烧碱是氢氧化钠的俗称,石灰水是氢氧化钙的水溶液,都具有腐蚀性;
二氧化硫能和氢氧化钠反应生成亚硫酸钠和水,二氧化碳能和氢氧化钠反应生成碳酸钠和水,一氧化碳不能和氢氧化钠反应.
解答 解:A、浓硫酸具有强氧化性,能够氧化纸张,而浓盐酸不具有强氧化性,因此浓硫酸能使纸张炭化,而浓盐酸不能,该选项说法不正确;
B、氧气不能燃烧,因此不能用作燃料,该选项说法不正确;
C、烧碱是氢氧化钠的俗称,石灰水是氢氧化钙的水溶液,都具有腐蚀性,该选项说法正确;
D、二氧化硫能和氢氧化钠反应生成亚硫酸钠和水,二氧化碳能和氢氧化钠反应生成碳酸钠和水,因此可以用氢氧化钠溶液吸收二氧化硫和二氧化碳,但是不能用氢氧化钠溶液吸收一氧化碳,该选项说法不正确.
故选:C.
点评 本题主要考查物质的性质,只有掌握了物质的性质,才能够对各种问题作出正确的解答.

练习册系列答案
相关题目
12. 烧杯中盛有CuCl2和HCl的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )
烧杯中盛有CuCl2和HCl的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )
 烧杯中盛有CuCl2和HCl的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )
烧杯中盛有CuCl2和HCl的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )| A. | ab段反应产生蓝色沉淀 | B. | bc段溶液增加70.2g | ||
| C. | c点对应的溶质质量分数为4.9% | D. | d点溶液显碱性 |
10.下列物质中,属于氧化物的是( )
| A. | NaCl | B. | Al2O3 | C. | NaOH | D. | H2SO4 |
14.实验室制取下列气体:①用锌和稀硫酸制取氢气;②用双氧水和二氧化锰制取氧气;③用石灰石和稀盐酸制取二氧化碳气体.下列有关说法错误的是( )
| A. | 都不需要对气体发生装置加热 | B. | 都不能用排水法收集气体 | ||
| C. | 都可用向上排空气法收集气体 | D. | 都可以用相同的发生装置 |
11.小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质的质量分数为10%,具体是什么物质无法辨认.老师告诉他,这瓶溶液可能是氢氧化纳、氯化钠、氢氧化钙或是碳酸钠中的一种.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是Ca(OH)2微溶于水,常温下不可能得到10%的氢氧化钙溶液.
(2)小亮取少量样品于试管中,滴加无色酚酞 试液,试液变红色,该溶液不可能是NaCl(填写化学式),理由是NaCl溶液呈中性,不能使无色酚酞试液变红色.
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告.
【设计实验方案】方案甲:选择氯化钙溶液来确定该溶液的成份;方案乙:选择稀盐酸来确定该溶液的成份.
【进行实验】你愿意选择方案乙(选填“甲”或“乙”)进行实验.
(4)玉鹏同学认为还可以用一种不同于甲、乙类别的物质来确定,请你帮他完成,该物质可以为石灰水.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是Ca(OH)2微溶于水,常温下不可能得到10%的氢氧化钙溶液.
(2)小亮取少量样品于试管中,滴加无色酚酞 试液,试液变红色,该溶液不可能是NaCl(填写化学式),理由是NaCl溶液呈中性,不能使无色酚酞试液变红色.
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告.
【设计实验方案】方案甲:选择氯化钙溶液来确定该溶液的成份;方案乙:选择稀盐酸来确定该溶液的成份.
【进行实验】你愿意选择方案乙(选填“甲”或“乙”)进行实验.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加氯化钙溶液(或稀盐酸). | 产生白色沉淀(或有气泡冒出) | 该溶液是碳酸钠溶液. 有关反应的化学方程式为: CaCl2+Na2CO3=CaCO3↓+2NaCl(或Na2CO3+2HCl=2NaCl+H2O+CO2↑). |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加该物质 | 产生白色沉淀 | 该溶液是碳酸钠溶液.有关反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH |

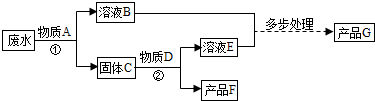 某厂排放的废水中含有硫酸铜,将废水处理可得到铜和铁红(氧化铁)两种产品,过程如图所示(废水中的其他物质不参与反应):
某厂排放的废水中含有硫酸铜,将废水处理可得到铜和铁红(氧化铁)两种产品,过程如图所示(废水中的其他物质不参与反应):