题目内容
18.镁是一种用途很广的金属,目前世界上 60%的镁是从海水中提取出来的.其重要步骤如下: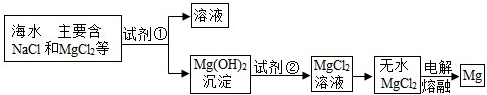
(1)上述步骤中试剂①应过量,理由是什么?
(2)写出 Mg(OH)2沉淀与试剂②发生反应的化学方程式.
分析 (1)根据步骤中试剂①应过量,目的是确保海水中的氯化镁完全反应进行分析;
(2)根据氢氧化镁和盐酸反应生成氯化镁和水进行分析.
解答 解:(1)步骤中试剂①应过量,目的是确保海水中的氯化镁完全反应;
(2)氢氧化镁和盐酸反应生成氯化镁和水,化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O;
故答案为:(1)将MgCl2全部转化成沉淀;(2)Mg(OH)2+2HCl=MgCl2+2H2O.
点评 本题是对海水中物质的提纯应用的考查,主要是利用了酸碱盐之间的相关反应,解决了物质的相关转化,是复分解反应发生条件和质量守恒定律的具体应用.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
9.氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe2O3、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如图:

(1)请写出步骤一中发生反应的化学方程式:MgO+2HCl═MgCl2+H2O(任写一个)
(2)溶液A中所含的阳离子有Mg2+、Fe3+、Cu2+、H+(填离子符号)
(3)已知:部分金属阳离子以氢氧化物形成沉淀时溶液的pH见表
步骤二中加入熟石灰,调节溶液的pH范围为6.7~9.1
(4)3个步骤中均用到的操作是过滤
(5)步骤三中生成产品的化学方程式为MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2.

(1)请写出步骤一中发生反应的化学方程式:MgO+2HCl═MgCl2+H2O(任写一个)
(2)溶液A中所含的阳离子有Mg2+、Fe3+、Cu2+、H+(填离子符号)
(3)已知:部分金属阳离子以氢氧化物形成沉淀时溶液的pH见表
| 沉淀物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
| 开始沉淀 | 1.9 | 4.2 | 9.1 |
| 完全沉淀 | 3.2 | 6.7 | 11.1 |
(4)3个步骤中均用到的操作是过滤
(5)步骤三中生成产品的化学方程式为MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2.
6.某碳酸钙和氧化钙组成的混合物中钙元素的质量分数为 60%,将 50g 混合物高温煅烧至质量不再改变,则生成二氧化碳的质量是( )
| A. | 6 g | B. | 8 g | C. | 13.2 g | D. | 20 g |
13.一定质量的物质甲(相对分子质量是 90)在氧气中完全燃烧,消耗了 6.4g 氧气,同时生成了 5.6g CO、4.4g CO2和 5.4g H2O,则下列对甲的说法中正确的是( )
| A. | 只含有碳、氢两种元素 | |
| B. | 一定含有碳、氢元素、可能含有氧元素 | |
| C. | 碳元素的质量分数为40% | |
| D. | 若相同质量的甲在 8.6g氧气中完全燃烧,只生成二氧化碳和水 |
3.下列物质中不存在分子这种微粒的是( )
| A. | 氯化钠溶液 | B. | 氦气 | C. | 氧气 | D. | 液氮 |
7.如图为初中化学常见气体的发生、收集装置.有关这些装置的说法不正确的是( )


| A. | 装置Ⅰ可作为加热固体制取气体的发生装置 | |
| B. | 装置Ⅱ可用于制取二氧化碳气体,不可以用于制取氧气 | |
| C. | 装置Ⅲ、Ⅳ可用于收集密度与空气密度差距较大,且不与空气中各成分反应的无毒气体 | |
| D. | 装置Ⅳ、Ⅴ都可用于实验室收集氧气 |
8.向一定质量的AgNO3和Fe(NO3)2的混合溶液中加入m克Zn粉,充分反应后过滤,将滤渣洗涤、干燥后称量,得到的固体质量为m克.据此,下列说法不正确的是( )
| A. | 滤渣中的物质至少有两种 | |
| B. | 取反应后的滤液滴加稀盐酸,有白色沉淀产生 | |
| C. | 取滤渣滴加稀盐酸,一定有气泡产生 | |
| D. | 取反应后的滤液观察,滤液可能呈浅绿色 |
 如图所示,小明和小红在做金属活动性顺序的探究实验,他们将铁钉加入到硫酸铜溶液中,观察到铁钉表面有气泡产生,一段时间后,在铁钉表面附着了红色的固体.
如图所示,小明和小红在做金属活动性顺序的探究实验,他们将铁钉加入到硫酸铜溶液中,观察到铁钉表面有气泡产生,一段时间后,在铁钉表面附着了红色的固体.