��Ŀ����
6����ľ����ũ�ҷ��ϣ���Ҫ�����Σ���ش�������⣮�����ᴿ��
��1�����ձ����һ�����IJ�ľ�ң�����ˮ��ͬʱ�ò��������裮������Һ����Ҫ���еĽ�����������K+��
��2�����ձ��еIJ�ľ����ͬ����Һһ����ˣ� �����Һ��Ȼ���ǣ������ķ����ǻ�����װ�����¹��ˣ�
��3������Һ��������������ȣ��ò��������裮���������н϶��������ʱ��ֹͣ���ȣ�
�ɷ�̽����
ȡ��3�����õľ�����������ˮ���ֵ���֧�Թ��У�
��4����һ֧���μ����ᣬ������ʹ�����ʯ��ˮ����ǵ����壮��д����ѧ����ʽ��
�ټ����K2CO3+2HCl=2KCl+CO2��+H2O��
�ڲ������ǣ�CO2+Ca��OH��2�TCaCO3��+H2O��
��5���ڶ�֧���μӷ�̪��Һ����Һ��Ϊ��ɫ��˵����Һ�ʼ��ԣ�Ϊ֤����Һ�ʼ�������CO32-����ģ������Թ��м���CaCl2��Һ�������ԣ�����ʱ������Ӧ�ķ���ʽΪK2CO3+CaCl2�T2KCl+CaCO3����
���� ��1�����ݼ����е����ӷ�����
��2�����һ�ι��˲��ɾ��ٹ���һ�Σ�
��3�����������IJ���������
��4��������̼��ʹ�����ʯ��ˮ����ǣ����ݷ�Ӧ��������������д��ѧ����ʽ��
��5��������Һ��ʹ��̪��Һ���ɫ������CO32-����֤������
��� �⣺��1����ľ����ũ�ҷ��ϣ���Ҫ�����Σ�������Һ����Ҫ���еĽ�����������K+�����K+��
��2�����ձ��еIJ�ľ����ͬ����Һһ����ˣ����˺���Һ�Ի��ǣ�����ԭ������ֽ���𣨻�ʹ��Һ���еIJ��������������ձ����Ӷ�ʹ����Һ���ǣ���Һ�������ֽ��Ե����ʹ����Һ��δ������ֽ�Ĺ���ֱ�����£��ò�����ʹ��Һ��Ȼ���ǣ���ʢ����Һ���ձ����ɾ��ȣ�
�����ķ����ǻ�����װ�����¹��ˣ�
��3���ȵ��������г��ֽ϶����Ĺ���ʱ��ֹͣ���ȣ����������������ʹ��Һ���ɣ�����н϶����������
��4��������̼��ʹ�����ʯ��ˮ����ǣ�˵�����ɶ�����̼��֤����̼���λ�̼�����Σ���ϣ�5����֪Ϊ̼��أ�̼��������ᷴӦ�����Ȼ��ء�ˮ�Ͷ�����̼������ʽΪK2CO3+2HCl=2KCl+CO2��+H2O��������̼���������Ʒ�Ӧ����̼��ƺ�ˮ������ʽΪCa��OH��2+CO2=CaCO3��+H2O�����K2CO3+2HCl=2KCl+CO2��+H2O��CO2+Ca��OH��2�TCaCO3��+H2O��
��5��������Һ��ʹ��̪��Һ���ɫ��Ҫ��֤��Һ�ʼ�������CO32-����ģ���һҪ��֤����ȥ̼������ڶ�������������������֤����Һ������ԣ�����ѡ��CaCl2��Һ����Ӧ�ķ���ʽΪK2CO3+CaCl2=CaCO3��+2KCl�������Һ�ĺ�ɫ��ȥ������ʧ����������ɫ������˵����Һ�ʼ�������CO32-����ģ���ľ�ҳʼ��ԣ��̬������������ʷ�Ӧ���ͷŰ��������ͷ�Ч�������̬���ʲ������ľ�һ��ʹ�ã�
�𰸣�
��1��K+��
��2��������װ�����¹��ˣ�
��3���н϶����������
��4����K2CO3+2HCl�T2KCl+CO2��CO2+H2O
��CO2+Ca��OH��2�TCaCO3��+H2O
��5���죻 K2CO3+CaCl2�T2KCl+CaCO3��
���� ���⿼���˳�����������������ɷֵ�ȷ������ɴ��⣬�����������ʵ����ʽ��У�

| ʵ���¼��� | ��1�� | ��2�� | ��3�� | ��4�� | ��5�� | ��6�� |
| ����ϡ��������/g | 5 | 5 | 5 | 5 | 5 | 5 |
| ʣ���������/g | 9.35 | 8.70 | 8.05 | 7.40 | 6.75 | 6.75 |
��2�������ϱ����ݣ�С����õĻ�ͭ��Ʒ��ʵ�ʺ�ͭ��������Ϊ67.5%��
��3��ʵ�������С�����ʣ����Һ�����ԣ�����ʣ����Һ���������������������ȷ��0.1%��
| ������������; | B | �ճ������ | |
| O2��ȼ-�����и���� H2O2�ֽ�ų�O2-ʵ������O2 | �·���Բ�����-�����ͻ�ƾ���ϴ ��������ë֯��-ȡ��������ȼ����ζ | ||
| C | ��ȫ��ʶ | D | ��ѧ������ |
| סլʧ��ʱ��ˮ����-���Ϳ�ȼ���Ż�� Ƥ��մ��Ũ����-��ˮ��ϴ����Ϳ�������� | ά����A-ȱ��ʱ����Ѫ�� ���ࡢ������-������ȡ��Ӫ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | 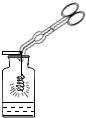 ��˿��������ȼ�� | B�� | 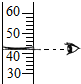 ��ȡҺ������ | ||
| C�� | 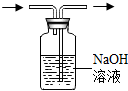 ��ȥCO�е�CO2 | D�� | 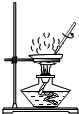 �����ᾧ |

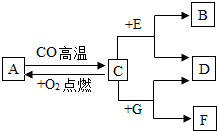 ����A��B��C��D��E��F��G�������ʣ�B�����嵥�ʣ�C��F�dz����Ľ���������FΪ��ɫ��DΪdz��ɫ��Һ��GΪ��ɫ��Һ������֮�������ͼ��ʾ��ϵ��
����A��B��C��D��E��F��G�������ʣ�B�����嵥�ʣ�C��F�dz����Ľ���������FΪ��ɫ��DΪdz��ɫ��Һ��GΪ��ɫ��Һ������֮�������ͼ��ʾ��ϵ��