题目内容
14.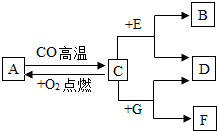 现有A、B、C、D、E、F、G七种物质,B是气体单质,C、F是常见的金属,其中F为红色,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图所示关系:
现有A、B、C、D、E、F、G七种物质,B是气体单质,C、F是常见的金属,其中F为红色,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图所示关系:(1)试推测下列物质的化学式:
BH2;DFeSO4.
(2)写出其中A转化成C的化学方程式:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2;
(3)写出C+G反应的化学方程式:Fe+CuSO4=FeSO4+Cu.
分析 根据“G是蓝色溶液”,可以确定G是铜盐的溶液,根据“D为浅绿色溶液”,说明D溶液中含有+2价铁,根据“B是气体单质,C、F是常见的金属,其中F为红色”,金属C和E反应生成D和气体单质B,根据质量守恒定律可知,C是铁,D是亚铁盐溶液,F是铜,E是盐酸或硫酸,B是氢气,又因为C和氧气燃烧生成A,说明A是四氧化三铁,然后再代入转化图中验证即可.
解答 解:根据“G是蓝色溶液”,可以确定G是铜盐的溶液,根据“D为浅绿色溶液”,说明D溶液中含有+2价铁,根据“B是气体单质,C、F是常见的金属,其中F为红色”,金属C和E反应生成D和气体单质B,根据质量守恒定律可知,C是铁,D是亚铁盐溶液,是硫酸亚铁或者氯化亚铁,F是铜,E是盐酸或者硫酸,B是氢气.而C和氧气燃烧生成A,说明A是四氧化三铁,四氧化三铁和一氧化碳在高温的条件下生成铁和二氧化碳,铁和氧气在点燃的条件下生成四氧化三铁,铁和铜盐反应生成亚铁盐和铜,铁和酸反应生成亚铁盐和氢气,推出的各种物质均满足题中的转化关系,推导正确.
(1)根据分析可知:B是H2,D是FeSO4;
(2)题中A转化成C,即四氧化三铁和一氧化碳反应生成铁和二氧化碳的反应是两种化合物生成了一种单质和一种化合物,不满足四大反应基本类型中的任意一种,符合题意,化学方程式为:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2;
(3)通过推导可知,C+G反应,即铁与铜盐反应生成亚铁盐和铜,故其反应的化学方程式为:Fe+CuSO4=FeSO4+Cu.
故答案为:
(1)H2,FeSO4;(2)Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2;(3)Fe+CuSO4=FeSO4+Cu.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

| A. | O2 | B. | K2SO3 | C. | Cu(OH)2 | D. | .KHSO4 |
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】
(1)6H2SO4(浓)+2Fe═Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产生可能有二氧化硫
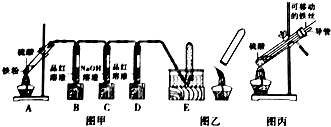
【实验探究】小明用图甲所示装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.
请帮助小明完成如表:
| 实验现象 | |||||
| 硫酸溶液浓度 | B中品红溶液 | D中品红溶液 | 爆鸣实验 | A中生成气体成分 | |
| 实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | SO2和H2 |
| 实验三 | 25% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
【交流反思】
(1)写出实验三中铁与硫酸溶液反应的化学方程式Fe+H2SO4═FeSO4+H2↑,写出实验二中发生爆鸣反应的化学方程式2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
(2)实验一中C装置的作用是吸收二氧化硫.【拓展延伸】小明又将A装置进行了如图丙所示的改进,试分析:增加的导管下端伸入液
面以下原因形成液封,防止生成的气体逸出,该导管所起的作用是平衡试管内外的压强,防止橡皮塞飞出.
| A. | 碘酒 | B. | 新鲜空气 | C. | 酱油 | D. | 蒸馏水 |

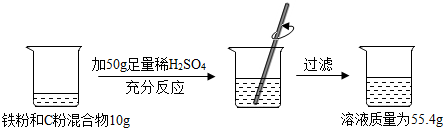
 某化学兴趣小组同学对某铜锌合金样品进行探究实验,称取样品10.0克放入烧杯中,再用100.0克稀硫酸溶液逐滴滴入,实验情况如图所示.
某化学兴趣小组同学对某铜锌合金样品进行探究实验,称取样品10.0克放入烧杯中,再用100.0克稀硫酸溶液逐滴滴入,实验情况如图所示. 某校综合实践活动小组在进行”诚信商品”研究时,检验商品标签所列成分及含量与事实是否相符,随机取出市售某纯碱样品(成分说明见图).经检验杂质仅是氯化钠.准确称取样品10.9克,加入50克氯化钙溶液使其充分反应(纯碱指碳酸钠),将反应生成的沉淀物经过滤,洗涤,干燥后得到白色固体10克.
某校综合实践活动小组在进行”诚信商品”研究时,检验商品标签所列成分及含量与事实是否相符,随机取出市售某纯碱样品(成分说明见图).经检验杂质仅是氯化钠.准确称取样品10.9克,加入50克氯化钙溶液使其充分反应(纯碱指碳酸钠),将反应生成的沉淀物经过滤,洗涤,干燥后得到白色固体10克.