题目内容
20. 汽泡爽是一种冲调饮料.其主要原料为柠檬酸(C6H8O7)和小苏打(NaHCO3);使用时将一包汽泡爽粉末倒入玻璃杯中,加入200mL冷水,看到有大量气泡快速生成,待粉末完全溶解,就得到一杯果味饮料.
汽泡爽是一种冲调饮料.其主要原料为柠檬酸(C6H8O7)和小苏打(NaHCO3);使用时将一包汽泡爽粉末倒入玻璃杯中,加入200mL冷水,看到有大量气泡快速生成,待粉末完全溶解,就得到一杯果味饮料.(1)柠檬酸(C6H8O7)由三种元素组成;其相对分子质量为:192;
(2)汽泡爽原料中的柠檬酸(C6H8O7)和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,请将其反应的化学方程式补充完整.3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3CO2↑
(3)所得饮料中能生成碳酸,所以又称为碳酸饮料,其原因是CO2+H2O=H2CO3(用化学方程式表示).
分析 (1)根据柠檬酸化学式的含义、相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据酸能与碳酸氢钠反应生成盐、水和二氧化碳,进行分析解答.
(3)根据二氧化碳与水反应生成碳酸,进行分析解答.
解答 解:(1)柠檬酸是由碳、氢、氧三种元素组成的;其相对分子质量为12×6+1×8+16×7=192.
(2)酸能与碳酸氢钠反应生成盐、水和二氧化碳,柠檬酸(C6H8O7)和小苏打(NaHCO3)粉末反应生成柠檬酸钠、水和二氧化碳,由质量守恒定律,反应前后氢原子的个数相等,反应前氢原子的个数为11,反应后氢原子的个数为5,则水的前面的化学计量数应为3,即补充的为3H2O.
(3)二氧化碳与水反应生成碳酸,反应的化学方程式为:CO2+H2O=H2CO3.
故答案为:(1)三;192;(2)3H2O;(3)CO2+H2O=H2CO3.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算、酸的化学性质、二氧化碳的化学性质等进行分析问题、解决问题的能力.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案
相关题目
8.善于用化学的视角看世界,能够提高我们的科学素养.你认为如表事实和相应的解释不一致的是( )
| 现象 | 解释(或结论) | |
| A | 氧气被压缩在氧气瓶中 | 压强增大,分子变小 |
| B | 向盛有某固体的烧杯中加入稀盐酸有气泡冒出 | 该固体一定是碳酸盐 |
| C | 石蜡燃烧生成水和二氧化碳 | 石蜡一定由碳、氢、氧元素组成 |
| D | a粒子轰击金箔,大部分穿过,极少数反弹回来 | 原子内部有很大的空隙 |
| A. | A | B. | B | C. | C | D. | D |
12.下列物质中,前者是氧化物,后者是化合物的是( )
| A. | 空气、氧气 | B. | 二氧化硫、高锰酸钾 | ||
| C. | 铁、氢气 | D. | 碳、水 |
9.下列实验方案正确的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 除去硫酸镁溶液中的硫酸 | 加入过量的Ba(OH)2溶液,过滤 |
| B | 分离氯化钠和硝酸钠固体混合物 | 加水溶解后,过滤,蒸发结晶 |
| C | 鉴别氯化铵和氯化钙 | 分别加入熟石灰,研磨,闻气味 |
| D | 鉴别羊毛织物和涤纶织物, | 分别灼烧,闻气味 |
| A. | A | B. | B | C. | C | D. | D |
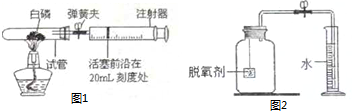 我校化学兴趣小组测定空气中氧气的含量,并改进教材方案.
我校化学兴趣小组测定空气中氧气的含量,并改进教材方案.
