题目内容
19.打开浓盐酸试剂瓶,发现瓶口有“白雾”出现.已知盐酸中含有水分子(H2O)、氢离子 (H+)和氯离子(Cl-).下列实验能证明“白雾”中含有氢离子的是( )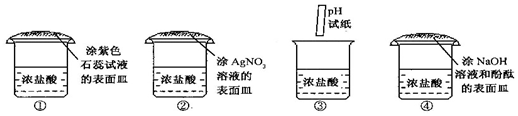
| A. | ①② | B. | ②④ | C. | ①③④ | D. | ①③ |
分析 证明“白雾”中含有氢离子即证明溶液呈酸性,所以能证明溶液呈酸性的反应就是证明了氢离子的存在,据此分析判断选项即可.
解答 解:浓盐酸瓶口的白雾是由浓盐酸挥发出的氯化氢气体与水蒸气结合而成的盐酸小液滴.
①石蕊试液遇酸性溶液变红色,涂有紫色石蕊的表面皿接触到“白雾”会变红,能证明“白雾”呈酸性,从而可说明溶液中含有氢离子.
②涂有硝酸银溶液的表面皿遇白雾会生成氯化银的白色沉淀,可说明白雾中含有氯离子.
③pH试纸可测量白雾的pH,从而可判断白雾(氯化氢与空气中的水蒸气结合成的盐酸小液滴)呈酸性,能证明氢离子的存在不能证明氯离子存在.
④氢氧化钠能使酚酞试液变红,涂有氢氧化钠和酚酞的表面皿显红色,盐酸的小液滴能与氢氧化钠反应,使溶液碱性消失红色褪去,从而可证明“白雾”呈酸性,含有氢离子,不能证明含有氯离子.
故①③④能证明“白雾”中含有氢离子.
故选:C.
点评 本题难度不大,掌握能证明溶液呈酸性(含有氢离子)的方法是正确解答本题的关键.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
4.酸、碱、盐溶解性表是学习化学的重要工具.下表列出了部分酸、碱、盐在20℃时的溶解性.利用此表完成下列各小题:
(1)查:CaSO4的溶解性微溶.
(2)碱和盐反应时,反应物必须都是可溶的.请写出一个碱和盐反应的化学方程式:2NaOH+CuSO4=Cu(OH)2↓+2Na2SO4.
| 离子 | OH- | Cl- | SO42- |
| H+ | 溶、挥 | 溶 | |
| Na+ | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 微 |
| Cu2+ | 不 | 溶 | 溶 |
(2)碱和盐反应时,反应物必须都是可溶的.请写出一个碱和盐反应的化学方程式:2NaOH+CuSO4=Cu(OH)2↓+2Na2SO4.
11. 现有HCl与CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X可能是下列物质中的( )
现有HCl与CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X可能是下列物质中的( )
 现有HCl与CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X可能是下列物质中的( )
现有HCl与CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X可能是下列物质中的( )| A. | 水 | B. | 纯碱溶液 | C. | 稀盐酸 | D. | 澄清石灰水 |
8.下列选项中的元素都属于非金属元素的是( )
| A. | H、S、P | B. | Ca、F、Cl | C. | O、I、Al | D. | C、K、N |
9.加油站应贴上的标志是( )
| A. |  | B. |  | C. |  | D. |  |
