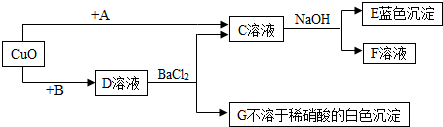
题目内容
7.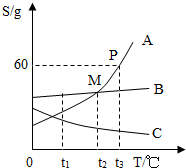 根据A、B、C三种物质的溶解度曲线,试回答下列问题:
根据A、B、C三种物质的溶解度曲线,试回答下列问题:(1)t1℃时,A、B、C三种物质的溶解度由大到小的顺序是B>A>C.
(2)点P的含义是:t3℃时,A物质的溶解度是60g.
(3)交点M的含义是:t2℃时,A、B物质的溶解度相等.
(4)t3℃时,50克水中最多溶解30克A物质.
(5)当A中含有少量B时,为了得到纯净的A,可采用降温结晶的方法.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,t1℃时,A、B、C三种物质的溶解度由大到小的顺序是:B>A>C;
(2)点P的含义是:t3℃时,A物质的溶解度是60g;
(3)交点M的含义是:t2℃时,A、B物质的溶解度相等;
(4)t3℃时,A物质的溶解度是60g,所以50克水中最多溶解30克A物质;
(5)A物质的溶解度受温度影响变化较大,所以当A中含有少量B时,为了得到纯净的A,可采用降温结晶的方法.
故答案为:(1)B>A>C;
(2)t3℃时,A物质的溶解度是60g;
(3)t2℃时,A、B物质的溶解度相等;
(4)30;
(5)降温结晶.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目
17.人体内一些液体的正常pH范围如下:①血浆(7.35-7.45)②胆汁(7.1-7.3)③胰液(7.5-8.0)④胃液(0.9一1.5)⑤唾液(6.6-6.9)上述液体中显酸性的是( )
| A. | ①② | B. | ②③ | C. | ③⑤ | D. | ④⑤ |
15.四个50mL烧杯中,分别放入浓度相同的20g盐酸,然后向这四份盐酸中分别加入足量的下列物质,经充分反应后都生成MgCl2,其中质量分数最大的是( )
| A. | Mg | B. | MgO | C. | Mg(OH)2 | D. | MgCO3 |
2.等质量的下列金属分别跟足量的稀硫酸反应,生成氢气最多的是( )
| A. | Mg | B. | Al | C. | Zn | D. | Fe |
19.水是万物之基,下列“水”可看作纯净物的是( )
| A. | 自来水 | B. | 矿泉水 | C. | 护城河水 | D. | 冰水 |