题目内容
6.欲将80g溶质质量分数为10%的硝酸钾溶液增浓至20%,可采用的方法是BA、向其中加入20g硝酸钾 B、向其中加入10g硝酸钾 C、倒掉40g10%的硝酸钾溶液 D、蒸发掉40g水.
分析 要使溶液的溶质质量分数变大,常通过两种方式:①加入溶质,②蒸发溶剂,据此结合溶质质量分数的计算进行分析判断.
解答 解:常通过两种方式:①加入溶质,②蒸发溶剂,
①加入硝酸钾:设需要加入硝酸钾的质量为a,则$\frac{80g×10%+a}{80g+a}$×100%=20%,a=10g即向其中加入10g硝酸钾;
②蒸发溶剂:设要蒸发水的质量为b,根据溶液稀释前后溶质的质量不变,则80g×10%=(80g-b)×20%,b=40g,即蒸发掉40g水.
故答案是:B、蒸发掉40g水.
点评 本题难度不是很大,考查溶液的浓缩问题,掌握溶液浓缩的方法、原理是正确解答此类题的关键所在.

练习册系列答案
相关题目
17.下列叙述正确的是( )
| A. | 结晶水合物是纯净物 | |
| B. | pH的大小可表示溶液的酸碱性强弱,它的数值不会等于零 | |
| C. | Na和Na+都是钠元素,它们的化学性质相同 | |
| D. | 5克胆矾溶于45克水中可制得质量分数为10%的硫酸铜溶液 |
14.碱式碳酸铝镁常用作塑料阻燃剂.
(1)碱式碳酸铝镁[MgaAlb(OH)c(CO3)d•xH2O]具有阻燃作用,是由于其受热分解需吸收大量热量和同时生成二氧化碳,受热分解后的固体产物中含有MgO和Al2O3(填写化学式).
(2)MgaAlb(OH)c(CO3)d•xH2O中a、b、c、d的代数关系式为2a+3b=c+2d.
(3)已知AlCl3+3NaOH=Al(OH)3↓+3NaCl;Al(OH)3+NaOH=NaAlO2+2H2O
某化学兴趣小组在实验室对碱式碳酸铝镁样品的成分进行验证,设计了如下实验方案
(1)碱式碳酸铝镁[MgaAlb(OH)c(CO3)d•xH2O]具有阻燃作用,是由于其受热分解需吸收大量热量和同时生成二氧化碳,受热分解后的固体产物中含有MgO和Al2O3(填写化学式).
(2)MgaAlb(OH)c(CO3)d•xH2O中a、b、c、d的代数关系式为2a+3b=c+2d.
(3)已知AlCl3+3NaOH=Al(OH)3↓+3NaCl;Al(OH)3+NaOH=NaAlO2+2H2O
某化学兴趣小组在实验室对碱式碳酸铝镁样品的成分进行验证,设计了如下实验方案
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验1 | 取样品少许加入足量稀HC1 | 样品全部溶解,有气泡产生 | 样品中含有CO32-离子 (填写化学式) |
| 实验2 | 取实验1反应后的溶液少许逐滴滴入足量 的NaOH溶液 | 一段时间后先产生沉淀,后部分沉淀溶解 | 固体中含有镁、铝元素 |
| … | |||
1.在生产生活中,很多问题都涉及化学知识,下列认识不正确的是( )
| A. | 工业“三废”和生活污水处理后再排放 | |
| B. | 为使农作物高产,大量施用化肥和农药 | |
| C. | 太阳能热水器既节能又环保 | |
| D. | 二氧化硫,二氧化氮,一氧化碳都是大气污染物 |
11.下列物质中,氮元素的质量分数最大的是( )
| A. | NH4HCO3 | B. | NH4Cl | C. | CO(NH2)2 | D. | NH4NO3 |
18.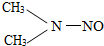 复旦大学投毒案中用的N-亚硝基二甲胺,又称二甲基亚硝胺,是一种半挥发性有机化学品,气味与味道很弱,易溶于水、醇、醚等,是一种有毒物品,具有强肝脏毒性,对人类很可能有致癌性.主要用于火箭燃料、抗氧剂等制造.其结构如图,对其认识错误的是( )
复旦大学投毒案中用的N-亚硝基二甲胺,又称二甲基亚硝胺,是一种半挥发性有机化学品,气味与味道很弱,易溶于水、醇、醚等,是一种有毒物品,具有强肝脏毒性,对人类很可能有致癌性.主要用于火箭燃料、抗氧剂等制造.其结构如图,对其认识错误的是( )
 复旦大学投毒案中用的N-亚硝基二甲胺,又称二甲基亚硝胺,是一种半挥发性有机化学品,气味与味道很弱,易溶于水、醇、醚等,是一种有毒物品,具有强肝脏毒性,对人类很可能有致癌性.主要用于火箭燃料、抗氧剂等制造.其结构如图,对其认识错误的是( )
复旦大学投毒案中用的N-亚硝基二甲胺,又称二甲基亚硝胺,是一种半挥发性有机化学品,气味与味道很弱,易溶于水、醇、醚等,是一种有毒物品,具有强肝脏毒性,对人类很可能有致癌性.主要用于火箭燃料、抗氧剂等制造.其结构如图,对其认识错误的是( )| A. | 该物质由四种元素组成 | B. | 该物质具有易燃性 | ||
| C. | 该物质应该密封保存 | D. | 该物质燃烧的产物中有氮气 |
15.鉴别日常生活中的下列各组物质,操作1和操作2均有错误的是( )
| 选项 | 鉴别的物质 | 操作1 | 操作2 |
| A | 软水和硬水 | 滴加肥皂水 | 加热蒸发 |
| B | 氯化钠和氢氧化钠 | 滴加盐酸 | 通入二氧化碳 |
| C | 氧气和二氧化碳 | 滴加紫色石蕊试液 | 伸入燃着的木条 |
| D | 真黄金和假黄金(铜锌合金) | 滴加稀盐酸 | 灼烧 |
| A. | A | B. | B | C. | C | D. | D |



