题目内容
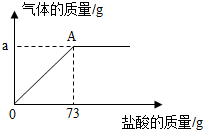 为了分析生铁中铁的含量,某学习小组进行了实验研究:取6g生铁与10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图(见图).(说明:生铁中杂质不溶于水,不与盐酸反应 )
为了分析生铁中铁的含量,某学习小组进行了实验研究:取6g生铁与10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图(见图).(说明:生铁中杂质不溶于水,不与盐酸反应 )(1)实验中可观察到
(2)铁完全反应用去盐酸的质量为
(3)生铁中铁的质量分数为
(4)A点表示的溶液的质量为多少?(写出求算过程)
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)铁与盐酸反应会生成氢气;
(2)从图示可得盐酸的质量;
(3)根据铁与盐酸反应的化学方程式,已知所用盐酸的质量和质量分数,能够计算出生铁中铁的质量分数;
(4)所得溶液质量应该是物质的总质量减去不溶性杂质和生成的气体的质量.
(2)从图示可得盐酸的质量;
(3)根据铁与盐酸反应的化学方程式,已知所用盐酸的质量和质量分数,能够计算出生铁中铁的质量分数;
(4)所得溶液质量应该是物质的总质量减去不溶性杂质和生成的气体的质量.
解答:解:(1)铁与盐酸反应会生成氢气,故可观察到有气体生成;
(2)铁完全反应用去盐酸的质量从图示中可以看出是73g;
(3)计算生铁中铁的质量分数,首先要算出纯铁的质量,再除以生铁的质量即可;
设与盐酸反应的铁的质量为x,氢气的质量为y
Fe+2HCl=FeCl2 +H2↑
56 73 2
x (73×10%)g y
=
,
=
x=5.6g,y=0.2g
生铁中铁的质量分数=
×100%=93.3%
答:生铁中铁的质量分数为93.3%
(4)生铁与盐酸刚好反应完全时所得溶液质量应是物质的总质量减去不溶性杂质和生成的气体的质量73g+6g-0.4g-0.2g=78.4g.
故答案为:(1)有气体生成;
(2)73;
(3)93.3%;
(4)答:A点表示的溶液的质量为78.4g;
(2)铁完全反应用去盐酸的质量从图示中可以看出是73g;
(3)计算生铁中铁的质量分数,首先要算出纯铁的质量,再除以生铁的质量即可;
设与盐酸反应的铁的质量为x,氢气的质量为y
Fe+2HCl=FeCl2 +H2↑
56 73 2
x (73×10%)g y
| 56 |
| 73 |
| x |
| 73g×10% |
| 73 |
| 2 |
| 73g×10% |
| y |
x=5.6g,y=0.2g
生铁中铁的质量分数=
| 5.6g |
| 6g |
答:生铁中铁的质量分数为93.3%
(4)生铁与盐酸刚好反应完全时所得溶液质量应是物质的总质量减去不溶性杂质和生成的气体的质量73g+6g-0.4g-0.2g=78.4g.
故答案为:(1)有气体生成;
(2)73;
(3)93.3%;
(4)答:A点表示的溶液的质量为78.4g;
点评:学会看曲线图是需要同学们掌握的一种技能,抓住起点,转折点和曲线的走势是关键.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
下列实验操作正确的是( )
A、 熄灭酒精灯 |
B、 倾倒液体 |
C、 气体验满 |
D、 液体过滤 |
绿色植物通过光合作用发生反应:CO2+H2O→葡萄糖+O2,由此推知葡萄糖( )
| A、只含碳、氢元素 |
| B、一定含碳、氢元素,可能含氧元素 |
| C、含有碳单质和水 |
| D、不能在氧气中燃烧 |
下列物质的用途与其依据的性质不相符的是( )
| A、金刚石用作钻探机的钻头--金刚石是天然存在的最硬的物质 |
| B、干冰用于人工降雨--干冰易升华,吸收大量的热 |
| C、石墨做电极--石墨很软 |
| D、二氧化碳用于灭火--二氧化碳不助燃、不可燃、密度比空气大 |
 水是生命之源.认识水资源、合理利用和保护水资源是我们义不容辞的责任.
水是生命之源.认识水资源、合理利用和保护水资源是我们义不容辞的责任.