题目内容
如图是一种医用药品瓶上的标签,试根据标签上的内容回答有关问题.
(1)请叙述“咀嚼”后咽下的好处 (答出一点即可).
(2)当胃酸(主要成分为盐酸)过多时,服用该药片后,在胃中可能发生的化学反应为 (用化学方程式表示).
(3)实际小苏打也可以治疗胃酸过多,但其不适合于胃溃疡患者,原因是 .
| 主要成分:氢氧化铝(大片状) 主治:胃痛、胃酸、 烧心等胃部不管症 用法:咀爵后咽下 |
(2)当胃酸(主要成分为盐酸)过多时,服用该药片后,在胃中可能发生的化学反应为
(3)实际小苏打也可以治疗胃酸过多,但其不适合于胃溃疡患者,原因是
考点:酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:(1)根据影响反应的因素来分析“咀嚼”后咽下的好处进行分析;
(2)根据氢氧化铝和盐酸反应生成氯化铝和水进行分析;
(3)根据反应的生成物来分析胃溃疡(胃黏膜溃烂)的病人胃酸过多时,不宜服用含碳酸盐的抗酸药的原因.
(2)根据氢氧化铝和盐酸反应生成氯化铝和水进行分析;
(3)根据反应的生成物来分析胃溃疡(胃黏膜溃烂)的病人胃酸过多时,不宜服用含碳酸盐的抗酸药的原因.
解答:解:(1)因嚼碎后与反应物胃酸的接触面积增大,化学反应加快,则嚼碎后服用疗效快;
(2)氢氧化铝与盐酸反应生成氯化铝和水,化学方程式为:Al(OH)3+3HCl=A1Cl3+3H2O;
(3)因碳酸盐与盐酸作用生成二氧化碳气体,能加重胃溃疡病情.
故答案为:(1)嚼碎后服用疗效快;
(2)Al(OH)3+3HCl=A1Cl3+3H2O;
(3)碳酸盐与盐酸作用生成二氧化碳气体,加重胃溃疡病情.
(2)氢氧化铝与盐酸反应生成氯化铝和水,化学方程式为:Al(OH)3+3HCl=A1Cl3+3H2O;
(3)因碳酸盐与盐酸作用生成二氧化碳气体,能加重胃溃疡病情.
故答案为:(1)嚼碎后服用疗效快;
(2)Al(OH)3+3HCl=A1Cl3+3H2O;
(3)碳酸盐与盐酸作用生成二氧化碳气体,加重胃溃疡病情.
点评:本题考查学生利用医用药品瓶上的标签来抽取信息,并利用物质的性质及物质之间的化学反应来分析解答问题.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
除去下列物质中的少量杂质,所选试剂及操作都正确的是( )
| 序号 | 物质 | 杂质 | 试剂 | 操作 |
| A | FeCl2溶液 | CuCl2 | 过量铁粉 | 结晶 |
| B | CO2 | H2O | 浓硫酸 | 洗气 |
| C | NaNO3溶液 | Na2CO3 | 适量CaCl2溶液 | 过滤 |
| D | 铜粉 | 铁粉 | 过量盐酸 | 过滤 |
| A、A | B、B | C、C | D、D |
属于化石燃料的物质是( )
| A、氢气 | B、煤 | C、木柴 | D、天燃气 |
化学就在我们身边,它能改善我们的生活.根据所学知识回答:若不小心被蚊虫叮咬(蚁虫能分泌出蚁酸),下列物质可用于涂抹以减轻疼痛的是( )
| A、食醋 | B、食盐水 |
| C、肥皂水 | D、氢氧化钠溶液 |
在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如表:
对该反应,下列描述中正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | 12 | 8 | 6 |
| 反应后质量/g | 4 | m | 28 | 2 |
| A、反应后m为10 |
| B、乙一定是该反应的催化剂 |
| C、反应中甲和丙的质量比为1:7 |
| D、该反应是化合反应 |
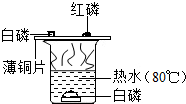 某同学为探究可燃物燃烧的条件,他查阅资料得知:白磷的着火点为40℃,红磷的着火点为240℃,它们在空气中燃烧都会产生白烟--五氧化二磷,五氧化二磷易溶于水,并能与水反应.
某同学为探究可燃物燃烧的条件,他查阅资料得知:白磷的着火点为40℃,红磷的着火点为240℃,它们在空气中燃烧都会产生白烟--五氧化二磷,五氧化二磷易溶于水,并能与水反应.
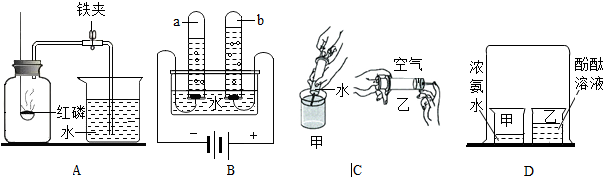
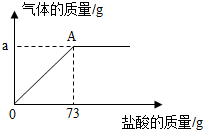 为了分析生铁中铁的含量,某学习小组进行了实验研究:取6g生铁与10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图(见图).(说明:生铁中杂质不溶于水,不与盐酸反应 )
为了分析生铁中铁的含量,某学习小组进行了实验研究:取6g生铁与10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图(见图).(说明:生铁中杂质不溶于水,不与盐酸反应 )