题目内容
如图中A、B、C、D、E是五种粒子的结构示意图,请回答下列问题:
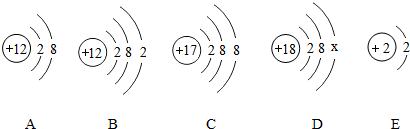
(1)D中x= ;
(2)图中A、B、C、D、E属于 种元素的粒子;
(3)A、B、C、D、E五种粒子中,不具备相对稳定结构的是 (填序号);
(4)A与C形成化合物的化学式是 .

(1)D中x=
(2)图中A、B、C、D、E属于
(3)A、B、C、D、E五种粒子中,不具备相对稳定结构的是
(4)A与C形成化合物的化学式是
考点:原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律
分析:(1)根据在原子中,核内质子数=核外电子数解答;
(2)依据质子数决定元素的种类,据此进行分析解答.
(3)根据最外层电子数决定元素的性质,最外层电子数是8(氦是2)属于稳定结构分析解答;
(4)A为镁离子,C为氯离子,A与C相互作用形成的化合物为氯化镁,写出其化学式即可.
(2)依据质子数决定元素的种类,据此进行分析解答.
(3)根据最外层电子数决定元素的性质,最外层电子数是8(氦是2)属于稳定结构分析解答;
(4)A为镁离子,C为氯离子,A与C相互作用形成的化合物为氯化镁,写出其化学式即可.
解答:解:
(1))在原子中,核内质子数=核外电子数,故X=18-2-8=8,故填:8;
(2)质子数决定元素的性质,ABCDE中粒子的质子数存在12、17、18、2四种,故其元素种类为四种;
(3)最外层电子数是8(氦是2)属于稳定结构,故ACDE属于稳定结构;不具备相对稳定结构的是B;
(4)由粒子结构示意图可知,A的质子数是12,核外电子数是10,为镁离子;C的质子数是17,核外电子数是18,为氯离子.镁离子与氯离子相互作用形成的化合物为氯化钠,其化学式为:MgCl2.
答案:
(1)8
(2)4
(3)B
(4)MgCl2.
(1))在原子中,核内质子数=核外电子数,故X=18-2-8=8,故填:8;
(2)质子数决定元素的性质,ABCDE中粒子的质子数存在12、17、18、2四种,故其元素种类为四种;
(3)最外层电子数是8(氦是2)属于稳定结构,故ACDE属于稳定结构;不具备相对稳定结构的是B;
(4)由粒子结构示意图可知,A的质子数是12,核外电子数是10,为镁离子;C的质子数是17,核外电子数是18,为氯离子.镁离子与氯离子相互作用形成的化合物为氯化钠,其化学式为:MgCl2.
答案:
(1)8
(2)4
(3)B
(4)MgCl2.
点评:本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如表:
对该反应,下列描述中正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | 12 | 8 | 6 |
| 反应后质量/g | 4 | m | 28 | 2 |
| A、反应后m为10 |
| B、乙一定是该反应的催化剂 |
| C、反应中甲和丙的质量比为1:7 |
| D、该反应是化合反应 |
元素周期表是学习化学的重要工具.如图是元素周期表中的一格,从中获取的信息错误的是( )
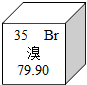

| A、通常状况下,该元素组成的单质呈液态 |
| B、该元素属于金属元素 |
| C、该元素的原子核外有35个电子 |
| D、该元素的相对原子质量为79.90 |
 用右图所示的实验装置制取二氧化碳一般有以下几个步骤,其正确的操作顺序是( )
用右图所示的实验装置制取二氧化碳一般有以下几个步骤,其正确的操作顺序是( )①向长颈漏斗中注入稀盐酸 ②向容器中放入几小块石灰石
③按要求装好仪器 ④检查装置的气密性 ⑤收集气体.
| A、①②③④⑤ |
| B、④③①②⑤ |
| C、③④②①⑤ |
| D、③④①②⑤ |
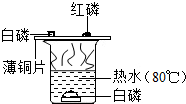 某同学为探究可燃物燃烧的条件,他查阅资料得知:白磷的着火点为40℃,红磷的着火点为240℃,它们在空气中燃烧都会产生白烟--五氧化二磷,五氧化二磷易溶于水,并能与水反应.
某同学为探究可燃物燃烧的条件,他查阅资料得知:白磷的着火点为40℃,红磷的着火点为240℃,它们在空气中燃烧都会产生白烟--五氧化二磷,五氧化二磷易溶于水,并能与水反应.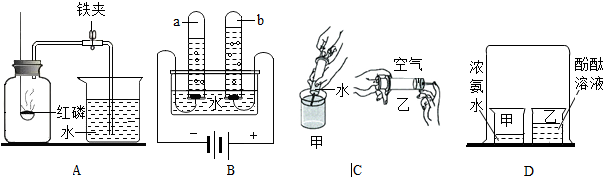
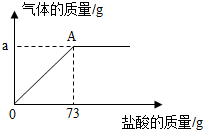 为了分析生铁中铁的含量,某学习小组进行了实验研究:取6g生铁与10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图(见图).(说明:生铁中杂质不溶于水,不与盐酸反应 )
为了分析生铁中铁的含量,某学习小组进行了实验研究:取6g生铁与10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图(见图).(说明:生铁中杂质不溶于水,不与盐酸反应 )