题目内容
19.下列各组物质的溶液,不能发生复分解反应的是( )| A. | HCl和Ca(OH)2 | B. | KCl和CuSO4 | C. | AgNO3和 BaCl2 | D. | H2SO4和Na2CO3 |
分析 发生复分解反应的基本条件是有沉淀生成、气体产生或有水生成,三个条件至少具备一个.
解答 解:A、反应方程式为 2HCl+Ca(OH)2=CaCl2+2H2O,生成了水,能发生复分解反应,故选项错误;
B、KCl和CuSO4相互交换成分没有沉淀、气体或水生成,不能发生复分解反应,故选项正确;
C、反应方程式为 2AgNO3+BaCl2=Ba(NO3)2+2AgCl↓,有沉淀生成,能发生复分解反应,故选项错误;
D、反应方程式为 Na2CO3+H2SO4=Na2SO4+CO2↑+H2O,有气体和水生成,能发生复分解反应,故选项错误;
故选:B.
点评 本题主要考查复分解反应发生的条件,所以要对常见的物质状态及水溶性必须熟悉.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9. 表格和图象能直观反应物质的变化规律.请根据下列表格和图象,回答有关问题:
表格和图象能直观反应物质的变化规律.请根据下列表格和图象,回答有关问题:
甲:氯化钠和氯化铵在不同温度时的溶解度
(1)由甲表中数据可知,溶解度受温度影响变化较大的物质是NH4Cl,氯化钠与氯化铵溶解度相等的温度范围在10~20℃之间.
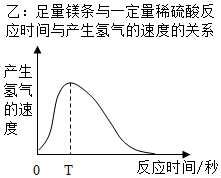
(2)镁与稀硫酸反应是放热反应.如乙图中从0到时间T产生氢气的速度逐渐增大,原因是镁与稀硫酸反应放热,加快反应速率,时间T后反应速度逐渐减小,逐渐减小的原因是随着反应的进行,稀硫酸浓度越来越低,反应越来越慢.
 表格和图象能直观反应物质的变化规律.请根据下列表格和图象,回答有关问题:
表格和图象能直观反应物质的变化规律.请根据下列表格和图象,回答有关问题:甲:氯化钠和氯化铵在不同温度时的溶解度
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| NH4Cl溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
| NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(2)镁与稀硫酸反应是放热反应.如乙图中从0到时间T产生氢气的速度逐渐增大,原因是镁与稀硫酸反应放热,加快反应速率,时间T后反应速度逐渐减小,逐渐减小的原因是随着反应的进行,稀硫酸浓度越来越低,反应越来越慢.
14.下列实验操作正确的是( )
| A. |  闻气味 | B. |  移动蒸发皿 | C. |  倾倒液体 | D. |  稀释浓硫酸 |
11. 如图是X、Y、Z三种固体物质的溶解度曲线,当它们的溶液接近饱和时,分别采用增加溶质、蒸发溶剂、升高温度三种方法,均可以变成饱和溶液的是( )
如图是X、Y、Z三种固体物质的溶解度曲线,当它们的溶液接近饱和时,分别采用增加溶质、蒸发溶剂、升高温度三种方法,均可以变成饱和溶液的是( )
 如图是X、Y、Z三种固体物质的溶解度曲线,当它们的溶液接近饱和时,分别采用增加溶质、蒸发溶剂、升高温度三种方法,均可以变成饱和溶液的是( )
如图是X、Y、Z三种固体物质的溶解度曲线,当它们的溶液接近饱和时,分别采用增加溶质、蒸发溶剂、升高温度三种方法,均可以变成饱和溶液的是( )| A. | Z溶液 | B. | Y溶液 | C. | X溶液 | D. | X、Y溶液 |


