题目内容
13.对比实验是化学学习中行之有效的思维方法,如图设计中能达到目的是(已知浓氨水显碱性,能使无色酚酞试液变红色)( )| A. | 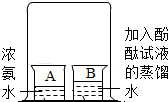 探究的是分子之间是否有间隔的 | |
| B. |  探究的是金属的锈蚀是否需要水 | |
| C. | 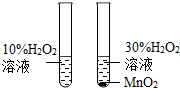 探究的是MnO2对H2O2分解的催化作用 | |
| D. |  探究的是可燃物燃烧是否需要与氧气充分接触 |
分析 微观粒子之间有间隔,总是不断运动的;
铁和水、氧气同时接触时容易生锈;
对比试验要确定好常量和变量.
解答 解:A、实验过程中,酚酞试液变红色,说明浓氨水中的氨分子是不断运动的,当运动到酚酞试液时,酚酞试液变红色,该选项探究的是分子是不断运动的,不是探究分子之间是否有间隔,该选项不能达到实验目的;
B、实验过程中,处在干燥空气中的铁钉不容易生锈,而处在潮湿空气中的铁钉容易生锈,因此该选项探究的是金属的锈蚀是否需要水,该选项能够达到实验目的;
C、如果探究的是MnO2对H2O2分解的催化作用,则过氧化氢溶液的浓度和体积应该相同,而过氧化氢溶液的浓度不同,因此该选项不能达到实验目的;
D、要探究可燃物燃烧是否需要与氧气充分接触,热水中的物质应该是白磷,该选项不能达到实验目的.
故选:B.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
4.下列关于空气及其成分的说法错误的是( )
| A. | 工业上可用分离液态空气法制氧气 | |
| B. | 利用氮气、氩气化学性质不活泼,作焊接金属的保护气 | |
| C. | 焊接金属时,用氧气作燃料 | |
| D. | 二氧化碳是植物进行光合作用的原料,可作温室的气体肥料 |
1.通过近期的学习,我们已经了解了常见金属的活动性顺序.铬(Cr)是重要的金属材料,在生产、生活中应用广泛.小华想金属活动顺序中没有铬,他和化学兴趣小组的同学们一起对Cr、Al、Cu的金属活动性顺序的相对位置进行了探究,过程如下:
【提出假设】根据已有的知识,对三种金属的活动性顺序提出了三种可能的假设:
a.Al>Cr>Cu b.Cr>Al>Cu c.Al>Cu>Cr.
【进行实验】取厚薄、形状、体积、大小完全相同,且用砂纸打磨过的三种金属薄片,然后分别 放入试管中,再分别倒入10mL等浓度的足量稀盐酸,观察现象,记录如下:
上述实验使用等浓度的盐酸溶液的理由是盐酸的浓度不同,会影响反应产生的气体的速率.
【得出结论】原假设中正确的是:a(填假设中a、b或c),写出铬与盐酸反应的化学方程式(铬与盐酸反应后显+2价):Cr+2HCl═CrCl2+H2↑.
【反思与评价】同学们认为只用三种药品也可以证明这三种金属的活动性顺序,这三种药品是铬、AlCl3溶液、CuCl2 溶液(或铬、Al2(SO4)3溶液、CuCl2 溶液,
或铝、铜、CrCl2溶液)(只需填写药品的一种组合方案即可).
【结论应用】根据探究结果,在CuCl2和A1C13的混合液中加入一定量的金属铬粉末,充分反应后过滤,向滤出的固体中加入盐酸,无明显现象,则滤液中一定含有溶质的化学式是AlCl3、CrCl2.
【提出假设】根据已有的知识,对三种金属的活动性顺序提出了三种可能的假设:
a.Al>Cr>Cu b.Cr>Al>Cu c.Al>Cu>Cr.
【进行实验】取厚薄、形状、体积、大小完全相同,且用砂纸打磨过的三种金属薄片,然后分别 放入试管中,再分别倒入10mL等浓度的足量稀盐酸,观察现象,记录如下:
| 金属 | Cr | A1 | Cu |
| 与盐酸发生反应的现象 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生激烈,金属迅速溶解 | 无明显现象 |
【得出结论】原假设中正确的是:a(填假设中a、b或c),写出铬与盐酸反应的化学方程式(铬与盐酸反应后显+2价):Cr+2HCl═CrCl2+H2↑.
【反思与评价】同学们认为只用三种药品也可以证明这三种金属的活动性顺序,这三种药品是铬、AlCl3溶液、CuCl2 溶液(或铬、Al2(SO4)3溶液、CuCl2 溶液,
或铝、铜、CrCl2溶液)(只需填写药品的一种组合方案即可).
【结论应用】根据探究结果,在CuCl2和A1C13的混合液中加入一定量的金属铬粉末,充分反应后过滤,向滤出的固体中加入盐酸,无明显现象,则滤液中一定含有溶质的化学式是AlCl3、CrCl2.
8.下列关于能源的叙述正确的是( )
| A. | 人类需要的能量都是由化学反应产生的 | |
| B. | 煤和石油都是可再生能源 | |
| C. | 大气污染,因此使用天然气可以避免污染 | |
| D. | 目前没有大量使用氢能源,是由于氢气的制取成本高,储存困难 |
18.下列过锃中,一定发生化学变化的是( )
| A. | 蜡烛熔化 | B. | 汽油挥发 | C. | 纸张燃烧 | D. | 海水晒盐 |
2.2015年10月5日浙江绍兴一化工厂因硝基氯苯车间反应引起爆炸.硝基氯苯化学式C6H4ClNO2,关于硝基氯苯的说法正确的是( )
| A. | 硝基氯苯中氢元素的质量分数比氮元素大 | |
| B. | 硝基氯苯是由碳、氢、氯、氮、氧五种元素组成 | |
| C. | 硝基氯苯是属于氧化物 | |
| D. | 硝基氯苯是由6个碳原子、4个氢原子、1个氯原子、1个氮原子和2个氧原子构成 |
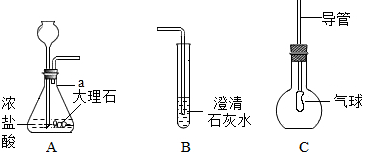 如图为某同学在实验室制取CO2并检验CO2性质的实验装置图.
如图为某同学在实验室制取CO2并检验CO2性质的实验装置图. 如图所示都是常见的日常生活用品,其中是有机高分子材料的有:③⑥(填序号).生活中要鉴别羊毛衫和合成纤维,可通过燃烧法的方法.
如图所示都是常见的日常生活用品,其中是有机高分子材料的有:③⑥(填序号).生活中要鉴别羊毛衫和合成纤维,可通过燃烧法的方法.