题目内容
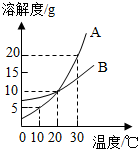 如图是A、B两种物质的溶解度曲线,下列叙述错误的是( )
如图是A、B两种物质的溶解度曲线,下列叙述错误的是( )| A、30℃时,向100克水中加入30克A物质,充分溶解后所得溶液是饱和溶液 |
| B、A物质的饱和溶液从30℃降温到10℃,变成不饱和溶液 |
| C、B物质的饱和溶液从30℃降温到20℃,其溶质质量分数减小 |
| D、20℃时,A、B物质的溶解度相同 |
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:根据溶解度曲线的意义结合溶解度曲线和溶质质量分数的计算分析解答即可.
解答:解:A、30℃时,A的溶解度是20g,向100克水中加入30克A物质,充分溶解后所得溶液是饱和溶液,正确;
B、A物质的饱和溶液从30℃降温到10℃,溶解度由20g变为5g,则须析出15g溶质,溶液仍为饱和溶液,错误;
C、B物质的饱和溶液从30℃降温到20℃,析出溶质,其溶质质量分数减小,正确;
D、20℃时,A、B物质的溶解度相同,正确;
故选B.
B、A物质的饱和溶液从30℃降温到10℃,溶解度由20g变为5g,则须析出15g溶质,溶液仍为饱和溶液,错误;
C、B物质的饱和溶液从30℃降温到20℃,析出溶质,其溶质质量分数减小,正确;
D、20℃时,A、B物质的溶解度相同,正确;
故选B.
点评:掌握溶解度曲线的意义是正确解答本题的关键.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
25℃时,向100g溶质质量分数为a%的氯化钠溶液中加入bg硝酸钾固体,恢复到原温度,结果有晶体析出.下列说法中错误的是( )
| A、该溶液的总质量一定小于(100+b)g |
| B、50 g该溶液中溶解有0.5a g氯化钠 |
| C、25℃时,该溶液一定是氯化钠的不饱和溶液 |
| D、25℃时,该溶液一定是硝酸钾的饱和溶液 |
下列原子结构示意图中,表示元素周期表中同一横行的原子是( )

| A、②③ | B、②④ | C、①② | D、①④ |
同学们,生活中下列活动主要体现了化学变化的是( )
| A、圣诞做贺卡 |
| B、寒假去滑霄 |
| C、除夕放鞭炮 |
| D、春节走亲戚 |

 设计了实验方案,进行了如图所示实验,并查阅资料得知:Na2CO3溶液和澄清石灰水都呈性(pH>7),CaCl2溶液呈中性(pH=7).
设计了实验方案,进行了如图所示实验,并查阅资料得知:Na2CO3溶液和澄清石灰水都呈性(pH>7),CaCl2溶液呈中性(pH=7).