题目内容
某种氮气中可能源有CO2、CO、H2,及水蒸气中的一种或几种,为了验证其组成,设计如下装置进行实验

(1)若将气体样品透过该实验装置,观察到的现象为:
①A中出现浑浊,②B中变蓝色,③C中无明显现象,④D中黑色粉末变红色,⑤E中出现浑浊,⑥F中变蓝色,根据上述现象,可以得出的结论是该氮气中一定混有(写气体的化学式) .
(2)上述实验无法确定某些气体是否存在.
①不一定存在 .原因是 .
②不一定存在 .原因是 .
(3)如果要验证N2中可能混有的所有气体是否存在,应该在上述实验装置中补充盛NaOH溶液的洗气瓶G,再重新连接,正确的连接顺序是:气体→ → → → →D→ → .

(1)若将气体样品透过该实验装置,观察到的现象为:
①A中出现浑浊,②B中变蓝色,③C中无明显现象,④D中黑色粉末变红色,⑤E中出现浑浊,⑥F中变蓝色,根据上述现象,可以得出的结论是该氮气中一定混有(写气体的化学式)
(2)上述实验无法确定某些气体是否存在.
①不一定存在
②不一定存在
(3)如果要验证N2中可能混有的所有气体是否存在,应该在上述实验装置中补充盛NaOH溶液的洗气瓶G,再重新连接,正确的连接顺序是:气体→
考点:常见气体的检验与除杂方法
专题:物质的检验、鉴别与推断
分析:二氧化碳能使澄清石灰水变浑浊,水能使无水硫酸铜变蓝,一氧化碳和氢气具有还原性,能与氧化铜反应生成铜.
解答:解:(1)(2)A中出现浑浊,说明气体中含有二氧化碳;B中白色粉末变成蓝色说明气体中含有水蒸气,但是由于是从石灰水中出来,无法确定原气体中是否含有水蒸气;C中黑色粉末变成红色,D中澄清石灰水变浑浊说明气体中一定含有一氧化碳,一氧化碳能与氧化铜反应生成铜和二氧化碳,二氧化碳能与氢氧化钙反应生成碳酸钙和水;因为气体是从澄清石灰水中出来的,所以不能确定是否含有氢气.
(3)要验证N2中可能混有的所有气体是否存在,应该在上述实验装置中补充盛NaOH溶液的洗气瓶G,并且用浓硫酸干燥气体.正确的顺序是气体→A→G→C→B→D→C→F.
故填:
(1)CO、CO2.
(2)①水蒸气;气体从石灰水中出来,无法确定原气体中是否含有水蒸气;
②氢气;经过灼热的氧化铜后,气体是从澄清石灰水中出来的,所以不能确定是否含有氢气.
(3)A→G→C→B→D→C→F.
(3)要验证N2中可能混有的所有气体是否存在,应该在上述实验装置中补充盛NaOH溶液的洗气瓶G,并且用浓硫酸干燥气体.正确的顺序是气体→A→G→C→B→D→C→F.
故填:
(1)CO、CO2.
(2)①水蒸气;气体从石灰水中出来,无法确定原气体中是否含有水蒸气;
②氢气;经过灼热的氧化铜后,气体是从澄清石灰水中出来的,所以不能确定是否含有氢气.
(3)A→G→C→B→D→C→F.
点评:浓硫酸、无水硫酸铜、氢氧化钠溶液、澄清石灰水是实验中经常用到的物质,对于它们的特性同学们一定要熟记与心.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
下列说法正确的是( )
| A、分子是保持物质性质的一种微粒 |
| B、原子核一定都是由质子和中子构成 |
| C、水结成冰后体积变大是由于水分子体积变大引起的 |
| D、同种元素的化合价在同一种物质中可能不同 |
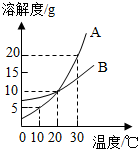 如图是A、B两种物质的溶解度曲线,下列叙述错误的是( )
如图是A、B两种物质的溶解度曲线,下列叙述错误的是( )| A、30℃时,向100克水中加入30克A物质,充分溶解后所得溶液是饱和溶液 |
| B、A物质的饱和溶液从30℃降温到10℃,变成不饱和溶液 |
| C、B物质的饱和溶液从30℃降温到20℃,其溶质质量分数减小 |
| D、20℃时,A、B物质的溶解度相同 |
质子数不同、电子数相同的两种粒子,它们不可能是( )
| A、同种元素的原子和离子 |
| B、一种元素的离子和另一种元素的原子 |
| C、两种不同元素的离子 |
| D、一种阳离子和一种阴离子 |
下列设计方案及结论均合理的是( )
| A、证明氯化钡溶液与硫酸钠溶液反应:将两种混合,有白色沉淀产生,说明反应发生 |
| B、证明某地雨水为酸雨:用pH测定雨水样品的pH=6.35,说明该雨水为酸雨 |
| C、证明二氧化碳中混有少量的一氧化碳气体:将混合气体点燃,气体能燃烧并发出蓝色火焰,说明含有一氧化碳 |
| D、证明某无色溶液是碱溶液:取样少许,向该无色溶液中加入酚酞试液,溶液变红,说明该溶液是碱溶液 |


