题目内容
钢铁是重要的金属材料,在生产、生活中有广泛的用途.
(1)每年世界上钢铁的产量很高,请以赤铁矿为例,写出工业炼铁的原理: ,该反应不是置换反应的理由是 .
(2)为了防止钢铁锈蚀,人们常采用在其表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法.这些方法都能防止锈蚀的共同原理是 .
(1)每年世界上钢铁的产量很高,请以赤铁矿为例,写出工业炼铁的原理:
(2)为了防止钢铁锈蚀,人们常采用在其表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法.这些方法都能防止锈蚀的共同原理是
考点:铁的冶炼,金属锈蚀的条件及其防护,置换反应及其应用
专题:金属与金属材料
分析:(1)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,写出反应的化学方程式即可.置换反应是单质与化合物反应生成另外的单质和化合物的化学反应;
(2)铁在与水和氧气并存时易生锈;防锈就是破坏铁生锈的条件.
(2)铁在与水和氧气并存时易生锈;防锈就是破坏铁生锈的条件.
解答:解:(1)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO
2Fe+3CO2.由化学方程式可知,反应物中没有单质,故不属于置换反应;故填:Fe2O3+3CO
2Fe+3CO2;反应物中没有单质;
(2)在其表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法都是使铁与氧气、水隔绝,故填:隔绝氧气和水.
(化学方程式(2分),其余每空(1分),共4分)
(1)Fe2O3+3CO
2Fe+3CO2 反应物均为化合物
(2)隔绝了水和氧气
| ||
| ||
(2)在其表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法都是使铁与氧气、水隔绝,故填:隔绝氧气和水.
(化学方程式(2分),其余每空(1分),共4分)
(1)Fe2O3+3CO
| ? |
| 高温 |
(2)隔绝了水和氧气
点评:本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 “鸟巢”被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE膜,并采用新一代的氮化镓铟高亮度LED材料.有关说法正确的是( )
“鸟巢”被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE膜,并采用新一代的氮化镓铟高亮度LED材料.有关说法正确的是( )| A、合金的熔点通常比组分金属高,硬度比组分金属小 |
| B、己知镓(Ga)原子最外电子层上有3个电子,可推知氮化镓化学式为Ga3N2 |
| C、工业上用金属铝与V2O5冶炼金属钒 |
| D、ETFE膜[CH2-CH2-CF2-CF2]是天然材料 |
下列有关燃烧与灭火的说法不正确的是( )
| A、用灯帽盖灭酒精灯--隔绝氧气 |
| B、镁条在酒精灯火焰上点燃--提高着火点 |
| C、森林灭火时,建立隔离带--隔绝可燃物 |
| D、家具起火,用水扑灭--降低温度 |
下列说法正确的是( )
| A、分子是保持物质性质的一种微粒 |
| B、原子核一定都是由质子和中子构成 |
| C、水结成冰后体积变大是由于水分子体积变大引起的 |
| D、同种元素的化合价在同一种物质中可能不同 |
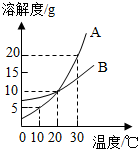 如图是A、B两种物质的溶解度曲线,下列叙述错误的是( )
如图是A、B两种物质的溶解度曲线,下列叙述错误的是( )| A、30℃时,向100克水中加入30克A物质,充分溶解后所得溶液是饱和溶液 |
| B、A物质的饱和溶液从30℃降温到10℃,变成不饱和溶液 |
| C、B物质的饱和溶液从30℃降温到20℃,其溶质质量分数减小 |
| D、20℃时,A、B物质的溶解度相同 |


