题目内容
13.氢氧化钠溶液与稀盐酸发生中和反应时观察不到明显现象,为了确定其反应是否发生,某班同学设计了不同的实验方案进行探究:(1)方案一:向装有一定量氢氧化钠溶液的烧杯中滴几滴酚酞试液,不断滴入稀盐酸,用玻璃棒搅拌.如果实验现象是溶液由红色变为无色,就可以证明氢氧化钠溶液与稀盐酸发生了化学反应,其反应的化学方程式是2NaOH+H2SO4=Na2SO4+2H2O.
(2)方案二:向装有一定量稀盐酸的试管中滴加氢氧化钠溶液,振荡后再向其中滴加碳酸钠溶液,如果有气泡产生,则说明氢氧化钠溶液与稀盐酸没有发生化学反应.你认为此结论正确吗?不正确,理由是硫酸剩余也会产生气泡.
(3)下列实验方案中,能证明氢氧化钠溶液与稀盐酸发生了反应的是A(填序号)
A.PH试纸测定氢氧化钠溶液的PH值,然后滴加稀盐酸,PH值逐渐减小,最终小于7
B.向一定量氢氧化钠溶液中滴加稀硫酸后,再滴加硫酸铜溶液,有蓝色沉淀生成.
分析 (1)酚酞遇碱变红色,遇酸、盐不变色,酸碱会发生中和反应生成盐和水.
(2)可以从硫酸过量也会产生气泡等原因进行分析解答.
(3)A、测量反应后的酸碱性与原溶液的酸碱性比较分析;
B、硫酸不足时,氢氧化钠有剩余就会生成蓝色沉淀.
解答 解:(1)酚酞遇碱变红色,遇酸、盐不变色,氢氧化钠是碱会使酚酞变红,滴入硫酸后,两者发生中和反应生成硫酸钠和水,不会使酚酞变色,故答案为:①溶液由红色变为无色,②2NaOH+H2SO4=Na2SO4+2H2O;
(2)硫酸和氢氧化钠反应后,硫酸过量,滴入碳酸钠溶液也会产生气泡,故答案为:不正确,硫酸剩余也会产生气泡;
(3)A、氢氧化钠的PH值大于7,滴入硫酸后,溶液PH值逐渐减小,最终小于7说明两者发生了化学反应,故A正确;
B、如果两者发生了化学反应,但是硫酸不足,氢氧化钠有剩余,也会生成蓝色沉淀,故B错误.
故选:A
点评 本题主要考查了利用反应现象和能量变化来分析中和反应是否发生,综合性较强.

练习册系列答案
相关题目
3. 在学校的国庆联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠
在学校的国庆联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠
(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小军对此很感兴趣,于是,进行探究.
[提出问题]过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜想]①可能有一种气体和另一种物质生成
②反应过程中可能有能量变化
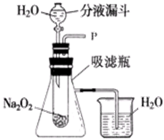
[设计装置]如图所示
[实验探究]
实验一:探究反应后生成的气体是什么?
(1)打开图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星
的木条靠近P处,木条复燃.说明生成的气体是氧气
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:过氧化钠与水反应放出热量,使吸滤瓶中的空气受热膨胀,因此伸入烧杯中的导管口看到有气泡产生;
实验二:继续探究反应后生成的另一种物质是什么?
(1)小张猜想另一种物质是Na2CO3,小军认为不可能.小军的依据是:根据质量守恒定律,反应物中没有碳元素,所以生成物中不可能有Na2CO3;
为了证实小军的看法,请你帮助设计一个证明Na2CO3不存在的实验.从资料中查阅知道:Na2CO3与稀盐酸反应会产生二氧化碳.
(2)小军从资料中查阅知道:若向含有OH-的溶液中滴入无色酚酞试液,就会出现红色.于是他取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色,说明反应后所得的剩余物中含有氢氧化钠(写物质名称或化学式).[表达]由实验探究的结果,写出过氧化钠和水反应的化学方程式:2Na202+2H2O═4NaOH+02↑.
 在学校的国庆联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠
在学校的国庆联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小军对此很感兴趣,于是,进行探究.
[提出问题]过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜想]①可能有一种气体和另一种物质生成
②反应过程中可能有能量变化
[设计装置]如图所示
[实验探究]
实验一:探究反应后生成的气体是什么?
(1)打开图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星
的木条靠近P处,木条复燃.说明生成的气体是氧气
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:过氧化钠与水反应放出热量,使吸滤瓶中的空气受热膨胀,因此伸入烧杯中的导管口看到有气泡产生;
实验二:继续探究反应后生成的另一种物质是什么?
(1)小张猜想另一种物质是Na2CO3,小军认为不可能.小军的依据是:根据质量守恒定律,反应物中没有碳元素,所以生成物中不可能有Na2CO3;
为了证实小军的看法,请你帮助设计一个证明Na2CO3不存在的实验.从资料中查阅知道:Na2CO3与稀盐酸反应会产生二氧化碳.
| 实验步骤 | 实验现象 | 实验结论 |
| 向反应后试管中的剩余物加适量的稀盐酸,并将可能产生的气体通入澄清石灰水中 | 若澄清石灰水变浑浊 实验中无此现象 | 说明碳酸钠存在 说明碳酸钠不存在 |
8.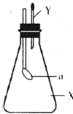 如图所示的锥形瓶内充满气体X,胶头滴管内盛有液体Y.挤压胶头滴管,使液体Y进入瓶中,振荡,一会儿可见套在玻璃管下端的小气球a鼓起.气体X和液体Y可能是( )
如图所示的锥形瓶内充满气体X,胶头滴管内盛有液体Y.挤压胶头滴管,使液体Y进入瓶中,振荡,一会儿可见套在玻璃管下端的小气球a鼓起.气体X和液体Y可能是( )
 如图所示的锥形瓶内充满气体X,胶头滴管内盛有液体Y.挤压胶头滴管,使液体Y进入瓶中,振荡,一会儿可见套在玻璃管下端的小气球a鼓起.气体X和液体Y可能是( )
如图所示的锥形瓶内充满气体X,胶头滴管内盛有液体Y.挤压胶头滴管,使液体Y进入瓶中,振荡,一会儿可见套在玻璃管下端的小气球a鼓起.气体X和液体Y可能是( )| A. | X是CO2,Y是KOH溶液 | B. | X是O2,Y是稀硫酸 | ||
| C. | X是H2,Y是NaOH溶液 | D. | X是CO,Y是稀盐酸 |
2.下列选项不属于化学这门学科研究范畴的是( )
| A. | 物质的组成与结构 | B. | 物质的性质与变化 | ||
| C. | 物质的运动状态 | D. | 物质的用途与制取 |
 高纯硅是制造计算机电路芯片的主要原料.请回答:
高纯硅是制造计算机电路芯片的主要原料.请回答:
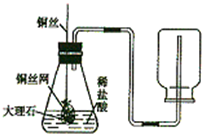 我们学习了实验室制取O2和CO2的方法,相信你能够回答下列间题.
我们学习了实验室制取O2和CO2的方法,相信你能够回答下列间题.