题目内容
10.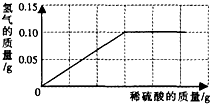 为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止.反应过程中生成的气体与所用硫酸溶液的质量关系如图所示.试计算:
为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止.反应过程中生成的气体与所用硫酸溶液的质量关系如图所示.试计算:(1)样品中铜的质量分数;
(2)反应所消耗的硫酸质量.
分析 根据锌与硫酸反应的化学方程式,由图中最多生成的氢气质量0.10g,可以计算出:(1)参加反应的锌的质量,进而计算出样品中铜的质量分数;
(2)参加反应的硫酸的质量,进而计算出硫酸溶液的质量;
解答 解:由图象可知反应完全后生成的氢气质量是0.1g
设样品中锌的质量为x;消耗硫酸溶液的质量为y;
Zn+H2SO4=ZnSO4+H2↑
65 98 2
x y×9.8% 0.10g
$\frac{65}{x}=\frac{98}{y×9.8%}=\frac{2}{0.10g}$
x=3.25g
y=50g
(1)样品中铜的质量分数=$\frac{10g-3.25g}{10g}$×100%=67.5%
(2)反应所消耗的硫酸溶液质量为y=50g;
答:(1)样品中铜的质量分数为67.5%;
(2)消耗硫酸溶液的质量为50g.
点评 解答本题的关键是根据图示知道生成氢气质量为0.10g,再根据氢气质量算出锌的质量,再计算铜的质量分数即可.

练习册系列答案
相关题目
18. 某校化学兴趣小组的同学采集到一种石灰石,他们取80g该样品进行煅烧实验(杂质不反应),测得反应后固体质量m与反应时间t的关系如表所示:
某校化学兴趣小组的同学采集到一种石灰石,他们取80g该样品进行煅烧实验(杂质不反应),测得反应后固体质量m与反应时间t的关系如表所示:
请回答下列问题:
(1)当石灰石完全反应后生成CO2的质量为22g.
(2)请在如图坐标图中画出煅烧时生成气体的质量m随时间t变化的曲线.
(3)求该石灰石中CaCO3的质量分数为多少g?
 某校化学兴趣小组的同学采集到一种石灰石,他们取80g该样品进行煅烧实验(杂质不反应),测得反应后固体质量m与反应时间t的关系如表所示:
某校化学兴趣小组的同学采集到一种石灰石,他们取80g该样品进行煅烧实验(杂质不反应),测得反应后固体质量m与反应时间t的关系如表所示:| 反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应后固体质量m/g | 80 | 75 | 70 | 66 | 62 | 58 | 58 |
(1)当石灰石完全反应后生成CO2的质量为22g.
(2)请在如图坐标图中画出煅烧时生成气体的质量m随时间t变化的曲线.
(3)求该石灰石中CaCO3的质量分数为多少g?
15.国际上提出了预防污染的新概念“绿色化学”,下列各项中,不属于“绿色化学”采取的措施的是( )
| A. | 利用垃圾发电,变废为宝 | |
| B. | 工业三废处理达标后再排放 | |
| C. | 多种植花草树木,禁止乱砍滥伐 | |
| D. | 为了减少污染物的排放,禁止开办化工厂 |
19.下列实验操作错误的是( )
| A. | 过滤时玻璃棒斜靠在三层滤纸一边 | |
| B. | 向锥形瓶中添加药品时,先加固体,后加液体 | |
| C. | 在烧杯中溶解氯化钠时用玻璃棒搅拌 | |
| D. | 制取氧气实验中,当导管口开始有气泡冒出时立即收集 |
20.某化学兴趣小组用化学方法测定一种钢样品中铁的含量.同学们称取了5.7g钢样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量也为10.0g)中.在化学反应过程中对烧杯(包括溶液和残余固体)进行了四次称量,记录如表:
(1)反应中产生氢气0.2g克,这种钢样品中铁的含量是多少?(精确到0.1%)
(2)钢的类型分为:含碳质量(C%)0.03%~0.3%为低碳钢;0.3%~0.6%为中碳钢;0.6%~2%为高碳钢.假设残留在烧杯中的黑色固体全部是炭,则这种钢属于高碳钢.
(3)有同学提出:灼烧可使钢中的炭变为CO2挥发掉,灼烧后钢样品质量会减轻.可是他们将一定量的钢样品灼烧后,发现质量反而增加了很多.原因是钢中含碳量少,碳减少的质量远小于铁转化为氧化物增加的质量.
| 反应时间 | t0 | t1 | t2 | t3 |
| 烧杯和药品质量/g | 25.7 | 25.6 | 25.5 | 25.5 |
(2)钢的类型分为:含碳质量(C%)0.03%~0.3%为低碳钢;0.3%~0.6%为中碳钢;0.6%~2%为高碳钢.假设残留在烧杯中的黑色固体全部是炭,则这种钢属于高碳钢.
(3)有同学提出:灼烧可使钢中的炭变为CO2挥发掉,灼烧后钢样品质量会减轻.可是他们将一定量的钢样品灼烧后,发现质量反而增加了很多.原因是钢中含碳量少,碳减少的质量远小于铁转化为氧化物增加的质量.
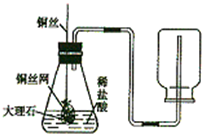 我们学习了实验室制取O2和CO2的方法,相信你能够回答下列间题.
我们学习了实验室制取O2和CO2的方法,相信你能够回答下列间题.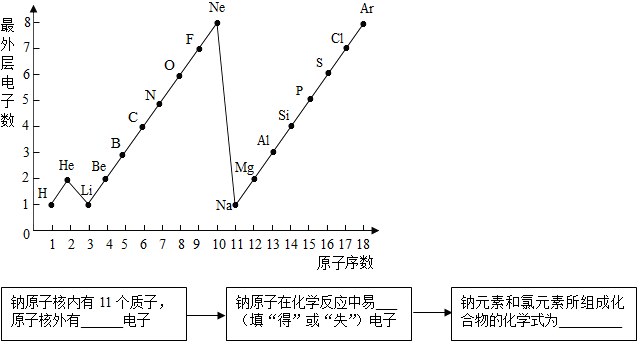
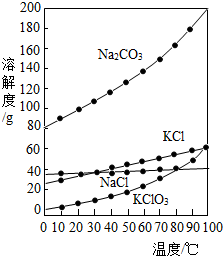 氯酸钾多用来制造火柴和烟花等.电解法是工业制造氯酸钾的主要方法:先电解热的氯化钠水溶液,电解的生成物烧碱和Cl2相互反应制得氯酸钠、氯化钠和水;再以氯酸钠和氯化钾为原料制备氯酸钾.
氯酸钾多用来制造火柴和烟花等.电解法是工业制造氯酸钾的主要方法:先电解热的氯化钠水溶液,电解的生成物烧碱和Cl2相互反应制得氯酸钠、氯化钠和水;再以氯酸钠和氯化钾为原料制备氯酸钾.