题目内容
 下面是利用如图装置完成验证二氧化碳性质的实验.
下面是利用如图装置完成验证二氧化碳性质的实验.(1)注射器1中盛有10mL水,注射器2中盛有10mL石蕊溶液,A中充满CO2,B中盛有NaOH溶液.先将K关闭,推注射器1向A中注入水,一段时间后,看到气球变鼓,再将注射器2中石蕊溶液注入A中,看到的现象是
(2)注射器1中盛有5mL的石灰水,注射器2中盛有10mLNaOH溶液,A中充满CO2,B中盛有稀盐酸(通常状况下,1体积的水约能溶解1体积二氧化碳).
①关闭K,将注射器2中的10mLNaOH溶液注入A中,轻轻振摇,看到的现象是
②对甲同学的猜想,乙同意认为不够准确,原因是
考点:碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的碱 碱的通性
分析:(1)根据二氧化碳能与水反应生成碳酸,碳酸显酸性能使石蕊变红色和容器内压强的改变来解答;
(2)根据二氧化碳能与氢氧化钠反应生成碳酸钠,能与氢氧化钙反应生成碳酸钙沉淀解答,碳酸钠能与氢氧化钙溶液反应生成碳酸钙沉淀,碳酸钠能与盐酸反应生成二氧化碳气体解答;
(3)气体参与反应导致容器内压强减小,碳酸钠能与石灰水反应生成白色沉淀、二氧化碳也能与石灰水反应生成白色沉淀;根据检验碳酸根存在的方法来分析.
(2)根据二氧化碳能与氢氧化钠反应生成碳酸钠,能与氢氧化钙反应生成碳酸钙沉淀解答,碳酸钠能与氢氧化钙溶液反应生成碳酸钙沉淀,碳酸钠能与盐酸反应生成二氧化碳气体解答;
(3)气体参与反应导致容器内压强减小,碳酸钠能与石灰水反应生成白色沉淀、二氧化碳也能与石灰水反应生成白色沉淀;根据检验碳酸根存在的方法来分析.
解答:解:(1)二氧化碳能溶于水,且与水反应生成碳酸,碳酸能使石蕊试液变红色;且容器内气体减少,压强减小,在外界气压的作用下,打开K会看到烧杯B中的溶液进入锥形瓶;故填:溶液变红色;二氧化碳与水反应生成碳酸,碳酸能使紫色的石蕊试液变红色;溶液沿导管进入锥形瓶;
(2)①二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,导致锥形瓶内的压强减小,外界空气由玻璃管进入气球,看到气球变大,若向外拉动注射器1,石灰水与碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠;故填:气球变鼓;溶液变浑浊;
②但是氢氧化钙溶液与二氧化碳反应也会出现碳酸钙白色沉淀,可以用加入盐酸的方法来检验是否有碳酸钠的存在,可打开K,在外界大气压的作用下,盐酸进入锥形瓶,若看到有气泡产生,则证明发生了反应.故填:二氧化碳也能使石灰水变浑浊;有气泡生成;Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(2)①二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,导致锥形瓶内的压强减小,外界空气由玻璃管进入气球,看到气球变大,若向外拉动注射器1,石灰水与碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠;故填:气球变鼓;溶液变浑浊;
②但是氢氧化钙溶液与二氧化碳反应也会出现碳酸钙白色沉淀,可以用加入盐酸的方法来检验是否有碳酸钠的存在,可打开K,在外界大气压的作用下,盐酸进入锥形瓶,若看到有气泡产生,则证明发生了反应.故填:二氧化碳也能使石灰水变浑浊;有气泡生成;Na2CO3+2HCl═2NaCl+H2O+CO2↑.
点评:本考点既考查了二氧化碳与碱反应的化学性质,也考查了质量守恒定律和实验设计中物理和化学的联系,综合性强.二氧化碳的化学性质和质量守恒定律的内容要记牢,有关理化合科的考点有:大气压强与化学反应的联系等,希望同学们好好把握.

练习册系列答案
相关题目
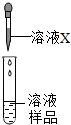
X溶液与AgNO3、Na2CO3、Na2SO4三种溶溶液发生反应均生成白色沉淀.则X可能是下列哪种物质的溶液( )
| A、HNO3 |
| B、HCl |
| C、BaCl2 |
| D、NaOH |
下列应用与化学方程式、基本反应类型都正确的是( )
| A、治疗胃酸过多症 2HCl+Ca(OH)2=CaCl2+2H2O 中和反应 |
| B、铁与稀硫酸反应制氯气 2Fe+3H2SO4=Fe2(SO4)3+3H2↑ 置换反应 |
| C、雨水呈酸性的原因 CO2+H2O=H2CO3 化合反应 |
| D、吸收二氧化气体 CO2+2NaOH=Na2CO3+H2O 复分解反应 |
 根据A物质和B物质的溶解度曲线(如图),回答下列问题:
根据A物质和B物质的溶解度曲线(如图),回答下列问题:

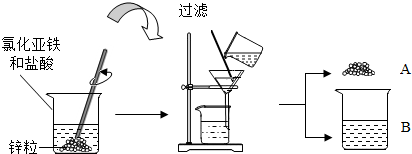
 溶液不是NaNO3,为确定其成分,某同学进行如下研究.
溶液不是NaNO3,为确定其成分,某同学进行如下研究.