题目内容
16.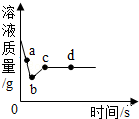 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量与加入Zn的质量(或反应时间)关系如图所示,下列说法正确的是( )
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量与加入Zn的质量(或反应时间)关系如图所示,下列说法正确的是( )| A. | 取a点溶液,滴加稀盐酸,无白色沉淀 | |
| B. | b点时溶液中金属离子有Zn2+、Cu2+,金属单质有Zn、Cu、Ag | |
| C. | 图标上b-c段质量增加的原因是Zn与Cu(NO3)2溶液反应 | |
| D. | c点和d点溶质种类不同,金属单质种类也不同 |
分析 根据金属与盐溶液的反应进行分析,在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,且置换时先把最弱的金属置换出来,并通过各反应的关系进行溶液质量的变化分析.
解答 解:在金属活动性顺序中,Zn>Cu>Ag,向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,与两种溶质依次发生反应
Zn+2AgNO3=Zn(NO3)2+2Ag
65 216
所以析出银的过程是溶液质量减少的过程;
Zn+Cu(NO3)2=Zn(NO3)2+Cu
65 64
所以析出铜的过程是溶液质量增加的过程
A、在a点时,硝酸银没有全部参加反应,溶液中含有硝酸银,滴加稀盐酸,会生成白色沉淀,故错误;
B、b点时金属单质中不含Zn,只含金属单质Ag,因为此时溶液中含金属离子Zn2+、Cu2+,故错误;
C、b-c段是锌和硝酸铜反应生成硝酸锌和铜,溶液质量增加,故正确;
D、c点和d点表示锌和硝酸铜完全反应,所以溶质种类相同,金属单质种类也相同,故错误.
故选:C.
点评 本题考查了金属活动性顺序的应用,要求学生熟悉金属的活动性顺序表,能利用活动性判断反应的发生,还要结合坐标分析各段的意义.

练习册系列答案
相关题目
6.下图分别表示四种化学实验操作,其中没有错误的是( )
| A. |  | B. |  | C. |  | D. |  |
7.茶叶中含有的茶氨酸(C7H14O3N2)可以降低血压、提高记忆力、保护神经细胞等.下列有关茶氨酸的说法中,正确的是( )
| A. | 茶氨酸属于氧化物 | |
| B. | 茶氨酸中碳元素与氢元素的质量比为6:1 | |
| C. | 茶氨酸中氧元素的质量分数最大 | |
| D. | 一个茶氨酸分子中含有一个氮分子 |
4.下列各组物质中,按照混合物、氧化物、碱的顺序排列的是( )
| A. | 加碘盐、水、纯碱 | B. | 稀有气体、干冰、熟石灰 | ||
| C. | 冰水混合物、液氧、火碱 | D. | 钢、高锰酸钾、氢氧化镁 |
1.食用纯碱的主要成分是碳酸钠,另外还含有少量的氯化钠:取13.5g样品放入烧杯中,每次加入20g稀盐酸(不考虑水、氯化氢逸出)后用精密仪器称量,记录实验数据如下:
(1)表中数据a=3.3g,b=4.95g.
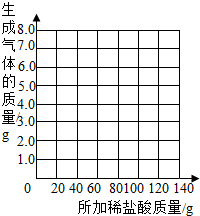
(2)请你在下边的坐标纸上绘制生成气体的质量与所加稀盐酸质量关系的曲线.
(3)计算所用稀盐酸的溶质质量分数.
| 加入盐酸的次数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 烧杯及所称物质总质量/g | 78.9 | 97.8 | 116.7 | 135.60 | 155.05 | 175.05 | 195.05 |
| 生成气体的质量/g | 1.1 | 2.2 | a | 4.4 | 4.95 | b | -- |
(2)请你在下边的坐标纸上绘制生成气体的质量与所加稀盐酸质量关系的曲线.

(3)计算所用稀盐酸的溶质质量分数.
8.下列反应的化学方程式正确的是( )
| A. | 锌和硫酸铜溶液:Zn+CuSO4=ZnSO4+Cu | |
| B. | 铁丝在纯氧中燃烧:2Fe+O2$\frac{\underline{\;燃烧\;}}{\;}$2FeO | |
| C. | 通电分解水:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2+O2 | |
| D. | 氯化钡溶液与硫酸钠溶液:NaSO4+BaCl2=BaSO4+2NaCl |
5.下列化学符号与含义相符的是( )
| A. | Cl2--两个氯原子 | B. | 3OH-1--三个氢氧根离子 | ||
| C. | KC1--氯化钾 | D. | 2SO3--两个三氧化硫分子 |
6.下列实验操作中错误的是( )
| A. |  液体的取用 | B. |  点燃酒精灯 | ||
| C. |  除去氢气中的水蒸气 | D. |  氧气验满 |

