题目内容
7.茶叶中含有的茶氨酸(C7H14O3N2)可以降低血压、提高记忆力、保护神经细胞等.下列有关茶氨酸的说法中,正确的是( )| A. | 茶氨酸属于氧化物 | |
| B. | 茶氨酸中碳元素与氢元素的质量比为6:1 | |
| C. | 茶氨酸中氧元素的质量分数最大 | |
| D. | 一个茶氨酸分子中含有一个氮分子 |
分析 A.根据氧化物的概念来分析;
B.根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断;
C.根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断;
D.根据分子的构成来分析.
解答 解:A.茶氨酸(C7H14O3N2)由四种元素组成,不属于氧化物,故错误;
B.茶氨酸中碳、氢元素的质量比为:(12×7):(1×14)=6:1,故正确;
C.茶氨酸中碳、氢、氧、氮元素的质量比为:(12×7):(1×14):(16×3):(14×2)=84:14:48:28,由此可知其中碳元素的质量分数最大,故错误;
D.茶氨酸是由茶氨酸分子构成的,茶氨酸分子是由碳原子、氢原子、氧原子和氮原子构成的,分子中不再含有分子,故错误.
故选B.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
17.如图是甲、乙两种微粒的结构示意图,下列有关说法错误的是( )
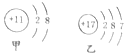
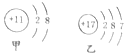
| A. | 粒子甲是金属阳离子,粒子乙是原子 | |
| B. | 粒子甲结构稳定,粒子乙易得电子 | |
| C. | 甲、乙两种元素属于同一周期 | |
| D. | 甲、乙两种微粒的化学性质均比较稳定 |
18.下列有关化学知识的应用、化学方程式、基本类型完全正确的一组是( )
| 物质的用途 | 化学方程式 | 基本类型 |
| A、用石灰石制生石灰 | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | 分解反应 |
| B、用盐酸除铁锈 | Fe+2HCl=Fe Cl2+H2↑ | 置换反应 |
| C、用红磷作发令枪子弹 | P+O2$\frac{\underline{\;点燃\;}}{\;}$PO2 | 化合反应 |
| D、一氧化碳用于炼铁 | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | 复分解反应 |
| A. | A | B. | B | C. | C | D. | D |
2.除去下列物质中的少量杂质(括号内为杂质)所用方法正确的是( )
| A. | ZnSO4溶液(CuSO4) 加入过量的锌粉,充分反应后过滤 | |
| B. | CaCl2固体(CaCO3) 加水溶解、过滤、洗涤、干燥 | |
| C. | NaCl溶液(CuSO4) 加入过量的氢氧化钠溶液,充分反应后过滤 | |
| D. | CO2溶液(CO) 点燃 |
12.下列物质的性质与用途的对应关系错误的是( )
| A. | 苏打可与盐酸反应,可用于治疗胃酸过多症 | |
| B. | 活性炭疏松多孔可用于吸附水中杂质 | |
| C. | 氮气的化学性质不活泼可作焊接金属的保护气 | |
| D. | 浓硫酸具有强吸水性,可用作干燥剂 |
19.在青海的茶卡盐湖,沿湖居民“夏天晒盐、冬天捞碱”,“盐”指的是食盐,“碱”指的是纯碱.以下是碳酸钠、氯化钠在不同温度下的溶解度
(1)“冬天捞碱”的原理是温度低于40℃时,随着温度降低,碳酸钠的溶解度减小.
(2)盐湖中获取的纯碱(天然碱)中一般含有一定量的氯化钠,现有标注为“纯度80%”的天然碱,要提纯碳酸钠,操作步骤如下:
①在50g40℃的热水中加入一定质量的天然碱,配成40℃时碳酸钠的饱和溶液;(不考虑不同溶质之间的相互影响)
②降温至10℃,析出一定质量的碳酸钠晶体,过滤,用少量水洗涤晶体;
③将碳酸钠晶体烘干后,获得18.3g碳酸钠粉末.(不考虑洗涤过程中碳酸钠的损耗)
(3)某学习小组同学要测定天然碱中碳酸钠的质量分数是否与标注符合,进行如下实验:
①称取5g天然碱放入锥形瓶内,再向其中加入50g溶质质量分数为10%的稀盐酸,充分反应后,称得烧杯内物质总质量为53.5g,请根据实验计算出天然碱中碳酸钠的质量分数.(结果保留到0.1%)
计算过程:
②思考:实验结果小于标注的原因可能是有部分二氧化碳溶于水或没有逸出锥形瓶.
(4)上述实验中所需的50g溶质质量分数为10%的稀盐酸,需要用市售的37%的浓盐酸进行配制.请计算出配制时需要浓盐酸13.5g、水36.5g.(结果保留至0.1)
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 80℃ | 100℃ | |
| S(Na2CO3)/g | 7.0 | 12.2 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 | 45.1 | 44.7 |
| S(NaCl)/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 38.4 | 39.8 |
(2)盐湖中获取的纯碱(天然碱)中一般含有一定量的氯化钠,现有标注为“纯度80%”的天然碱,要提纯碳酸钠,操作步骤如下:
①在50g40℃的热水中加入一定质量的天然碱,配成40℃时碳酸钠的饱和溶液;(不考虑不同溶质之间的相互影响)
②降温至10℃,析出一定质量的碳酸钠晶体,过滤,用少量水洗涤晶体;
③将碳酸钠晶体烘干后,获得18.3g碳酸钠粉末.(不考虑洗涤过程中碳酸钠的损耗)
(3)某学习小组同学要测定天然碱中碳酸钠的质量分数是否与标注符合,进行如下实验:
①称取5g天然碱放入锥形瓶内,再向其中加入50g溶质质量分数为10%的稀盐酸,充分反应后,称得烧杯内物质总质量为53.5g,请根据实验计算出天然碱中碳酸钠的质量分数.(结果保留到0.1%)
计算过程:
②思考:实验结果小于标注的原因可能是有部分二氧化碳溶于水或没有逸出锥形瓶.
(4)上述实验中所需的50g溶质质量分数为10%的稀盐酸,需要用市售的37%的浓盐酸进行配制.请计算出配制时需要浓盐酸13.5g、水36.5g.(结果保留至0.1)
16.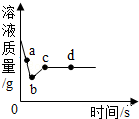 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量与加入Zn的质量(或反应时间)关系如图所示,下列说法正确的是( )
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量与加入Zn的质量(或反应时间)关系如图所示,下列说法正确的是( )
 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量与加入Zn的质量(或反应时间)关系如图所示,下列说法正确的是( )
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量与加入Zn的质量(或反应时间)关系如图所示,下列说法正确的是( )| A. | 取a点溶液,滴加稀盐酸,无白色沉淀 | |
| B. | b点时溶液中金属离子有Zn2+、Cu2+,金属单质有Zn、Cu、Ag | |
| C. | 图标上b-c段质量增加的原因是Zn与Cu(NO3)2溶液反应 | |
| D. | c点和d点溶质种类不同,金属单质种类也不同 |