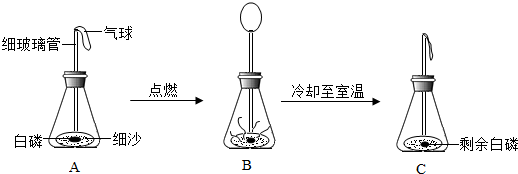
题目内容
17.某兴趣小组同学在实验室将一定量的稀硫酸加入到盛有氢氧化钠溶液的烧杯中,未看到明显的现象.部分同学产生疑问:酸和碱到底能不能发生反应?(1)该小组同学又做了如下实验:【实验步骤】向滴有酚酞溶液的稀氢氧化钠溶液的试管中,加入稀硫酸,并振荡.【实验现象】观察到溶液由红色变为无色.【实验结论】氢氧化钠和硫酸发生了反应.反的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O
(2)同学们对(1)实验后溶液中的溶质组成展开探究,做出如下猜想:
小明的猜想是:只有Na2SO4;
小亮的猜想是:有Na2SO4和NaOH;
小丽的猜想是:有Na2SO4和H2SO4;
你认为小亮的猜想不合理.理由是如果有NaOH存在,含有酚酞的溶液不能为无色
【拓展】若要验证余下两种猜想中的一种是正确的,请完成下面的实验方案.
| 实验步骤 | 预期实验现象 | 实验结论 |
| 取(1)实验后溶液少量于试管中加入①锌粒 | ②有气泡产生 (或没有气泡产生) | ③小丽 (或小明)的猜想正确 |
分析 (1)氢氧化钠溶液能够使酚酞变红,氢氧化钠和稀硫酸反应生成了硫酸钠和水,可以据此完成该题的解答;
(2)溶液变为了无色,说明不含有氢氧化钠,故可以判断小亮的猜想是错误的,而要验证小明和小丽的猜想只需验证是否含有硫酸即可,可以据此解答该题.
解答 解:(1)氢氧化钠溶液能够使酚酞变红,所以在加入稀硫酸之前溶液呈红色,当加入稀硫酸,由于氢氧化钠和稀硫酸反应生成了硫酸钠和水,而硫酸钠为中性的溶液,所以可以观察到溶液的红色消失,该反应的化学方程式为:H2SO4+2NaOH═Na2SO4+2H2O;
(2)溶液变为了无色,说明不含有氢氧化钠,故可以判断小亮的猜想是错误的,而要验证小明和小丽的猜想只需验证是否含有硫酸即可,根据硫酸的性质,可以选择活泼的金属来进行验证,例如锌,如果观察到有气泡冒出,则说明溶液中含有硫酸,反之则没有硫酸;
故答案为:(1)H2SO4+2NaOH═Na2SO4+2H2O;
(2)小亮;如果有NaOH存在,含有酚酞的溶液不能为无色;
【拓展】
| 实验步骤 | 预期实验现象 | 实验结论 |
| 取(1)实验后溶液少量于试管中加入①锌粒 | ②有气泡产生 (或没有气泡产生) | ③小丽 (或小明)的猜想正确 |
点评 在做中和反应的实验时,由于酸和碱的溶液一般是无色,二者反应时的现象不明显,所以往往借助于一些试剂或仪器等(如酸碱指示剂、pH试纸、温度计等),来帮助我们判断反应是否进行或恰好完全.

练习册系列答案
相关题目
8.为探究气体X的组成;某兴趣小组进行如图所示实验(固定装置未画出)
【资料在线】
(1)加热条件下,气体X能与氧化铜反应生成铜、水和氮气.
(2)碱石灰为固体氢氧化钠和氧化钙的混合物,不与气体X反应.
无水氯化钙可吸收气体X.
(3)本实验条件下,氮气密度为1.15g•L-1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计.
【实验步骤】
(1)连接仪器,并检查装置气密性.
(2)取一定量氧化铜,准确称得其质量为2.40g.
(3)按图所示装入药品,测量并记录相关数据Ⅰ(见表).
(4)连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热.当A装置中氧化铜反应完全,停止加热,继续通入气X至玻璃管冷却,再次测量并记录相关数据Ⅱ(见表).
【实验装置】

【相关数据】
【回答问题】
(1)B装置中氧化钙吸水的原理为CaO+H2O=Ca(OH)2(用化学方程式表示).
(2)实验过程中,当观察到,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是防止灼热的氧化铜被氧化和生成的水蒸气全部进入B装置内,使实验更精确.
(3)分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.
(4)通过计算推导出气体X的化学式NH3.
【资料在线】
(1)加热条件下,气体X能与氧化铜反应生成铜、水和氮气.
(2)碱石灰为固体氢氧化钠和氧化钙的混合物,不与气体X反应.
无水氯化钙可吸收气体X.
(3)本实验条件下,氮气密度为1.15g•L-1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计.
【实验步骤】
(1)连接仪器,并检查装置气密性.
(2)取一定量氧化铜,准确称得其质量为2.40g.
(3)按图所示装入药品,测量并记录相关数据Ⅰ(见表).
(4)连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热.当A装置中氧化铜反应完全,停止加热,继续通入气X至玻璃管冷却,再次测量并记录相关数据Ⅱ(见表).
【实验装置】

【相关数据】
| 数据编号 测量项目 | Ⅰ | Ⅱ |
| 玻璃管(含药品)的质量/g | 52.40 | 51.92 |
| B装置(含药品)的质量/g | 102.00 | 102.54 |
| 氮气的体积/mL | / | 243.5 |
(1)B装置中氧化钙吸水的原理为CaO+H2O=Ca(OH)2(用化学方程式表示).
(2)实验过程中,当观察到,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是防止灼热的氧化铜被氧化和生成的水蒸气全部进入B装置内,使实验更精确.
(3)分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.
(4)通过计算推导出气体X的化学式NH3.
6.常见原子团及化合价
| 原子团名称 | 原子团符号 | 化合价 |
| 硫酸根 | ||
| 碳酸根 | ||
| 氢氧根 | ||
| 硝酸根 | ||
| 铵根 |
3.下列关于分子、原子、离子这三种常见粒子的说法中正确的是( )
| A. | 热胀冷缩现象是因为粒子的体积增大的缘故 | |
| B. | 分子和原子的根本区别是分子可分而原子不可分 | |
| C. | 分子、原子都能保持物质的化学性质而离子不能保持物质的化学性质 | |
| D. | 离子都达到了稳定结构 |

 表示氢原子,
表示氢原子, 表示氧原子)
表示氧原子)
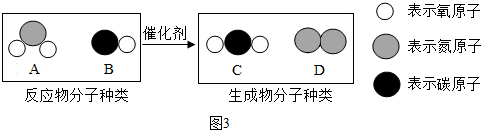

 (1)写出指定的仪器名称
(1)写出指定的仪器名称