题目内容
5.图示法是学习物质的组成和结构知识常用的一种形象化表示方法.(1)如图1示是五种粒子的结构示意图:

①图1中粒子共能表示4种元素.
②图1中表示的阳离子和阴离子相互间形成的化合物的化学式为MgCl2.
(2)图示2中能表示保持水的化学性质的粒子是D(
 表示氢原子,
表示氢原子, 表示氧原子)
表示氧原子)
(3)“三效催化转换器”可将汽车尾气中有毒气体处理为无毒气体,图3为该反应的微观示意图.
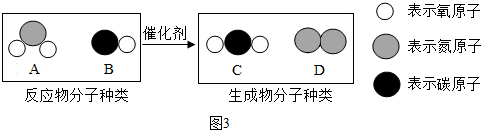
①图示中有4种物质,属于氧化物的是ABC(填图中字母).
②反应中,生成C和D的质量比为44:7.
(4)图4是元素周期表的一部分,请回答相关问题:

①氟元素与氯元素位于同一纵行的原因是原子最外层电子数相同,它们在化学反应中都易得到(填“得到”或“失去”)电子.
②M2-与Ne 核外电子排布相同,则M 元素的名称为氧.已知M 元素的相对原子质量为a,则M 元素原子核内的中子数为a-8.
分析 (1)根据微粒的结构示意图的意义分析判断回答;
(2)根据水的构成、分子的定义分析回答;
(3)根据反应的微观示意图.写出化学方程式,据此意义分析回答;
(4)①根据原子的最外层电子数目的特点分析;
②根据微粒的构成分析回答.
解答 解:(1)①图1中粒子共有四种质子数,能表示4种元素.
②由图1的粒子的结构示意图可知,表示的阳离子是镁离子,阴离子是氯离子,相互间形成的化合物是氯化镁,化学式为:MgCl2.
(2)水是由水分子构成的,D微粒能表示水分子,能保持水的化学性质;
(3)由反应的微观示意图可知,此反应的化学方程式为:2NO2+4CO $\frac{\underline{\;催化剂\;}}{\;}$4CO2+N2;
①图示中有4种物质,属于氧化物的是NO2、CO、CO2三种物质;
②反应中,生成C和D的质量比为 (44×4):28=44:7.
(4)①氟元素与氯元素位于同一纵行的原因是原子最外层电子数相同,最外层电子数是7 大于4,它们在化学反应中都易得到电子.
②M2-与Ne 核外电子排布相同,则M原子的质子数是8,元素的名称为氧.已知M 元素的相对原子质量为a,则M 元素原子核内的中子数为a-8.
故答为:(1)①4; ②MgCl2;(2)D;(3)①ABC,②44:7;(4)①原子最外层电子数相同得到电子,②氧 a-8.
点评 本题的难度不大,涉及的知识点较多,了解微粒结构示意图、微观模型图和元素周期表的意义是解答本题的基础知识.

练习册系列答案
相关题目
10.如表是我国部分城市空气质量周报,阅读并回答下列问题:
(1)最容易出现酸雨的城市是重庆.
为减少城市酸雨的产生,可采取的措施是①②④(填序号).
①少用煤作燃料②采用燃料脱硫技术 ③不必采取措施,无所谓 ④开发新能源
(2)控制城市汽车尾气对空气造成污染的方法是②③.
①禁止汽车上路 ②改良汽车的燃料及开发新能源
③加装尾气处理装置植树造林 ④戴呼吸面具.
| 城市 | 污染指数 | 首要污染物 | 空气质量级别 | 城市 | 污染指数 | 首要污染物 | 空气质量级别 |
| 北京 | 92 | TSP | Ⅱ | 济南 | 76 | TSP | Ⅱ |
| 天津 | 82 | TSP | Ⅱ | 武汉 | 83 | NOx | Ⅱ |
| 哈尔滨 | 96 | TSP | Ⅱ | 重庆 | 98 | SOx | Ⅱ |
| 上海 | 74 | NOx | Ⅱ | 贵阳 | 69 | TSP | Ⅱ |
| 注:TSP--空气中飘尘;NOx--氮的氧化物;SOx--硫的氧化物 | |||||||
为减少城市酸雨的产生,可采取的措施是①②④(填序号).
①少用煤作燃料②采用燃料脱硫技术 ③不必采取措施,无所谓 ④开发新能源
(2)控制城市汽车尾气对空气造成污染的方法是②③.
①禁止汽车上路 ②改良汽车的燃料及开发新能源
③加装尾气处理装置植树造林 ④戴呼吸面具.
17.某兴趣小组同学在实验室将一定量的稀硫酸加入到盛有氢氧化钠溶液的烧杯中,未看到明显的现象.部分同学产生疑问:酸和碱到底能不能发生反应?
(1)该小组同学又做了如下实验:【实验步骤】向滴有酚酞溶液的稀氢氧化钠溶液的试管中,加入稀硫酸,并振荡.【实验现象】观察到溶液由红色变为无色.【实验结论】氢氧化钠和硫酸发生了反应.反的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O
(2)同学们对(1)实验后溶液中的溶质组成展开探究,做出如下猜想:
小明的猜想是:只有Na2SO4;
小亮的猜想是:有Na2SO4和NaOH;
小丽的猜想是:有Na2SO4和H2SO4;
你认为小亮的猜想不合理.理由是如果有NaOH存在,含有酚酞的溶液不能为无色
【拓展】若要验证余下两种猜想中的一种是正确的,请完成下面的实验方案.
(1)该小组同学又做了如下实验:【实验步骤】向滴有酚酞溶液的稀氢氧化钠溶液的试管中,加入稀硫酸,并振荡.【实验现象】观察到溶液由红色变为无色.【实验结论】氢氧化钠和硫酸发生了反应.反的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O
(2)同学们对(1)实验后溶液中的溶质组成展开探究,做出如下猜想:
小明的猜想是:只有Na2SO4;
小亮的猜想是:有Na2SO4和NaOH;
小丽的猜想是:有Na2SO4和H2SO4;
你认为小亮的猜想不合理.理由是如果有NaOH存在,含有酚酞的溶液不能为无色
【拓展】若要验证余下两种猜想中的一种是正确的,请完成下面的实验方案.
| 实验步骤 | 预期实验现象 | 实验结论 |
| 取(1)实验后溶液少量于试管中加入①锌粒 | ②有气泡产生 (或没有气泡产生) | ③小丽 (或小明)的猜想正确 |
11.下列有关物质用途的叙述中,不正确的是( )
| A. | 食盐作调味品 | B. | 氧气用于急救病人 | ||
| C. | 甲醛用于浸泡食用的海产品 | D. | 碳酸氢钠作发酵粉 |