题目内容
7.如图是一个概念图,概念图在整理知识时是十分有用的.请在图中空白处填上恰当的内容.
分析 根据溶液的组成来解答,溶液分为溶质和溶剂,水是常见的溶剂;
解答 解:溶液有溶质和溶剂组成,常见的溶剂为水;
故答案为:溶质 水(答案合理即可).
点评 本题考查溶液的组成,溶液分为溶质和溶剂.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.为测定石灰石钙元素的质量分数,某同学取一定量该石灰石(杂质不含钙元素且不参加反应也不溶于水)研碎后直接煅烧一段时间后,称量剩余固体的质量为103g,向其加入500g质量分数为14.6%的稀盐酸恰好完全反应,过滤后称量剩余固体质量为25g,则该石灰石中钙元素的质量分数为( )
| A. | 28% | B. | 32% | C. | 40% | D. | 50% |
17.下列有关厨房里的说法正确的是( )
| A. | 切菜的刀钝了要磨一磨-为了减小压强 | |
| B. | 铝制品耐腐蚀-铝的化学性质稳定 | |
| C. | 揭开正在煮东西的锅盖时,会看到“白气”-气体的液化 | |
| D. | 煮粥时纯碱放多了加醋调节-发生了中和反应 |
15.很多水龙头是铜质镀铬的,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,同学们进行如下探究活动:
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…
铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【预测】三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮.
【回答问题】(1)用砂纸打磨金属片的目的是除去表面的氧化物.
(2)实验一所发生反应的化学方程式是Cr+H2SO4=CrSO4+H2↑.
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是铝和铬都能够和硫酸铜反应,无法比较铬和铝的金属活动性强弱.
(4)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是A1、CrSO4溶液、Cu.
【归纳】比较金属活动性强弱的方法有
①通过金属与酸反应快慢判断金属活动性强弱
②通过金属与盐溶液反应判断金属活动性强弱.
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…
铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【预测】三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮.
| 实验一 | 实验二 | 实验三 | |
| 实验 方案 |  |  |  |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色. | 铜片无明显现象 | 铝片表面产生气泡较快. |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢. | 铜不与稀硫酸反应 | 铝能和稀硫酸发生反应,反应速率较快 |
| 三种金属在金属活动性顺序中的相对位置关系是铝、铬、铜 | |||
(2)实验一所发生反应的化学方程式是Cr+H2SO4=CrSO4+H2↑.
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是铝和铬都能够和硫酸铜反应,无法比较铬和铝的金属活动性强弱.
(4)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是A1、CrSO4溶液、Cu.
【归纳】比较金属活动性强弱的方法有
①通过金属与酸反应快慢判断金属活动性强弱
②通过金属与盐溶液反应判断金属活动性强弱.
19.我国化学家侯德榜改革了国外的纯碱生产工艺,发明了联合制碱法,其生产流程可简要表示如下: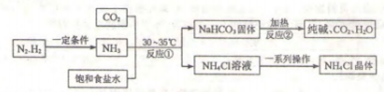
已知NH4Cl受热易分解,请回答下列问题.
(1)上述流程中可循环利用的物质是二氧化碳(写一种).
(2)反应②的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(3)下表是几种物质在不同温度下的溶解度.
分析表中数据可知,反应①中NaHCO3作为固体析出的原因是在室温时,碳酸氢钠的溶解度最小.上述流程中得到的NH4Cl溶液中一定有碳酸氢钠杂质,经一系列操作后,从NH4Cl溶液中获得NH4Cl晶体的方法是降温结晶.

已知NH4Cl受热易分解,请回答下列问题.
(1)上述流程中可循环利用的物质是二氧化碳(写一种).
(2)反应②的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(3)下表是几种物质在不同温度下的溶解度.
| 温度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | - | - | - | - | |
| NaHCO3 | 6.9 | 8.2 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - | |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.5 | 77.3 | |
17.要使如图中的气球鼓起来,则使用的固体和液体可以是( )
①石灰石和稀盐酸②镁和稀硫酸 ③氢氧化钠和水 ④生石灰和水.

①石灰石和稀盐酸②镁和稀硫酸 ③氢氧化钠和水 ④生石灰和水.
| A. | ①② | B. | ①②④ | C. | ①④ | D. | ①②③④ |
 我们的生活离不开空气.
我们的生活离不开空气.