题目内容
18.在生产、生活和科研中,需要经常用到各种干燥剂(除湿剂).(1)生石灰--白色块状固体,吸水后生成熟石灰,廉价易得,应用广泛.生石灰在物质分类上属于氧化物(选填“酸”、“碱”、“盐”或“氧化物”).
(2)浓硫酸--无色粘稠液体,有强烈的吸水性,常用于化学实验.日常生活中很少用它作干燥剂,主要原因是浓硫酸具有强烈的腐蚀性.
分析 (1)根据生石灰是氧化钙的俗称,是由钙元素和氧元素组成的,进行分析解答.
(2)根据浓硫酸具有强烈的腐蚀性,进行分析解答.
解答 解:(1)生石灰是氧化钙的俗称,是由钙元素和氧元素组成的化合物,属于氧化物.
(2)浓硫酸是无色粘稠液体,有强烈的吸水性,常用于化学实验.日常生活中很少用它作干燥剂,日常生活中很少用它作干燥剂,主要原因是浓硫酸具有强烈的腐蚀性.
故答案为:(1)氧化物;(2)浓硫酸具有强烈的腐蚀性.
点评 本题难度不大,掌握氧化物与酸碱盐的特征、浓硫酸具有强烈的腐蚀性是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.空气中体积分数约占21%的气体是( )
| A. | 氮气 | B. | 氧气 | C. | 二氧化碳 | D. | 稀有气体 |
6. 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质.其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.00g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.00g,再把100.00g稀盐酸平均分成四份依次加入样品中,实验数据记录如下:
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质.其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.00g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.00g,再把100.00g稀盐酸平均分成四份依次加入样品中,实验数据记录如下:
(1)分析表中数据数据X的值是204.48.
(2)请你通过计算说明该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
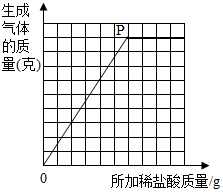
(3)根据实验数据,某同学在坐标纸上绘制出了所加稀盐酸质量与生成气体质量关系的曲线请你求出图中转折处P点的坐标.(保留一位小数)
 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质.其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.00g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.00g,再把100.00g稀盐酸平均分成四份依次加入样品中,实验数据记录如下:
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质.其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.00g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.00g,再把100.00g稀盐酸平均分成四份依次加入样品中,实验数据记录如下:| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 每次加盐酸前 烧杯及所盛物质的总质量/g | 158.00 | 181.24 | X | 228.60 |
| 所加盐酸的溶液质量/g | 25.00 | 25.00 | 25.00 | 25.00 |
| 充分反应后烧杯及所盛物质总质量/g | 181.24 | 204.48 | 228.60 | 253.60 |
| 每次生成的二氧化碳质量/g | 1.76 | 1.76 | Y | 0 |
(2)请你通过计算说明该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,某同学在坐标纸上绘制出了所加稀盐酸质量与生成气体质量关系的曲线请你求出图中转折处P点的坐标.(保留一位小数)
10.某同学想用实验证明FeCl3溶液显黄色不是Cl-离子造成的,下列实验无意义的是( )
| A. | 观察KCl溶液没有颜色 | |
| B. | 向FeCl3溶液中滴加适量氢氧化钠溶液,振荡后静置,溶液黄色消失 | |
| C. | FeCl3溶液中滴加适量无色硝酸银溶液,振荡后静置,溶液黄色未消失 | |
| D. | 加水稀释后FeCl3溶液黄色变浅 |
7.2012年2月某地发生了一起亚硝酸钠中毒事件.亚硝酸钠外观酷似食盐且有咸味,亚硝酸钠和食盐的有关资料如下:
根据上表提供的信息完成下列问题:
(1)写出亚硝酸钠的两条物理性质:易溶于水,熔点271℃.
(2)请你写出检验食盐中是否含有亚硝酸钠的过程(操作、现象、结论):取少量待测食盐与稀盐酸反应,若有红棕色气体产生,则该食盐中混有亚硝酸钠,反之则无;(或取待测食盐加热到320℃以上,若有臭味气体产生,则食盐中含有亚硝酸钠,反之则无).
| 项 目 | 亚硝酸钠(NaNO2) | 氯化钠(NaCl) |
| 水溶性 | 易溶,在15℃时溶解度为81.5克 | 易溶,在15℃时溶解度为35.8克 |
| 熔点 | 271℃ | 801℃ |
| 沸点 | 320℃会分解,放出有臭味的气体 | 1413℃ |
| 跟稀盐酸作用 | 放出红棕色的气体NO2 | 无反应 |
(1)写出亚硝酸钠的两条物理性质:易溶于水,熔点271℃.
(2)请你写出检验食盐中是否含有亚硝酸钠的过程(操作、现象、结论):取少量待测食盐与稀盐酸反应,若有红棕色气体产生,则该食盐中混有亚硝酸钠,反之则无;(或取待测食盐加热到320℃以上,若有臭味气体产生,则食盐中含有亚硝酸钠,反之则无).