题目内容
19.将一杯质量分数为13%的盐水倒去一半后,剩下的盐水质量分数为( )| A. | 13% | B. | 26% | C. | 52% | D. | 不一定 |
分析 盐是均匀的分散水中的,倒出一半后,剩下的盐水溶液的浓度仍然是13%,由此解答.
解答 解:溶液是均一的,倒出一半盐水溶液,剩下的部分浓度不会变化,仍是13%.
故选A.
点评 此题主要考查百分率的意义,注意“溶质是均匀的分散的溶剂中”,各部分的浓度是相同的

练习册系列答案
相关题目
10.实验表明,用碱性溶液浸泡新鲜的蔬菜,能有效除去蔬菜上的残留农药,从而降低对人体的损害.根据上述表明,对刚买回来的蔬菜,你认为应浸泡在下列哪种溶液中( )
| A. | 白酒 | B. | 碳酸钠溶液 | C. | 食醋 | D. | 烧碱溶液 |
7.金属钛(Ti)是重要的航空航天材料.Ti可以用TiO2与Si共熔制取,反应的化学方程式为:TiO2+Si$\stackrel{高温}{→}$SiO2+Ti.该反应中的还原剂是( )
| A. | Si | B. | TiO2 | C. | SiO2 | D. | Ti |
14.金属活动性顺序有重要的应用.
①将一段锌片插入到CuSO4溶液中,观察到明显的现象,反应的化学方程式为Zn+CuSO4=ZnSO4+Cu.
②金属分别与水、水蒸气的反应情况如下表:
根据金属活动性顺序和表中的信息,判断“镁与水蒸气”的反应情况为CD
(填写代号).
A.不反应 B.缓慢反应
C.比镁与冷水反应快 D.比铁与水蒸气反应快.
①将一段锌片插入到CuSO4溶液中,观察到明显的现象,反应的化学方程式为Zn+CuSO4=ZnSO4+Cu.
②金属分别与水、水蒸气的反应情况如下表:
| 物质 | 镁与冷水 | 铁与冷水 | 铁与水蒸气 | 铜与冷水 | 铜与水蒸气 |
| 反应情况 | 缓慢反应 | 不反应 | 能反应 | 不反应 | 不反应 |
(填写代号).
A.不反应 B.缓慢反应
C.比镁与冷水反应快 D.比铁与水蒸气反应快.
4.安德烈•盖姆和康斯坦丁•诺沃肖洛夫因在二维空间材料石墨烯的突破性实验而荣获2010年诺贝尔物理学奖.石墨烯是由碳原子构成的单层片状结构的新材料(结构示意图如下),可由石墨剥离而成,具有极好的应用前景.下列说法不正确的是( )
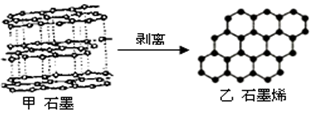

| A. | 石墨烯具有良好的导电性 | |
| B. | 石墨烯是一种有机化合物 | |
| C. | 石墨烯在空气中充分燃烧产物为二氧化碳 | |
| D. | 石墨烯与石墨具有相似的化学性质 |
9.除去保温瓶内壁上的水垢(主要含碳酸钙和氢氧化镁),最好选用( )
| A. | 浓硫酸 | B. | 浓盐酸 | C. | 氯化钠 | D. | 固体氢氧化钠 |
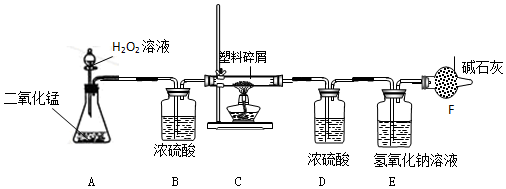
 如图为速力菲补血剂的说明书.
如图为速力菲补血剂的说明书.