题目内容
14.如图1是初中实验常见装置,请回答: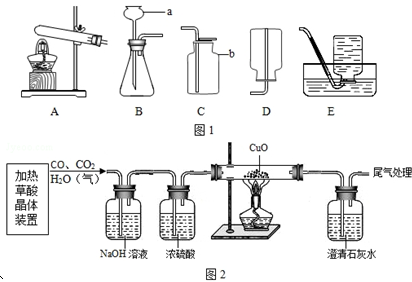
(1)写出图中标号为a、b的仪器名称:a长颈漏斗;b集气瓶.
(2)实验室中用过氧化氢溶液和二氧化锰混合制取氧气,发生装置应选用图中B(填字母代号)装置,收集氧气可选用C(或E)(填字母代号)装置,该反应的文字表达式为过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(3)某活动小组用加热草酸晶体制得的CO做还原氧化铜的实验,设计了如图2的装置.(化学方程式:H2C2O4˙2H2O $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+CO↑+3H2O)
回答下列问题:
①加热分解草酸晶体应选用的发生装置为A(填上面常见装置图中的字母代号).
②能证明氧化铜被还原的现象是黑色粉末变为红色.装氧氧化钠溶液的洗气瓶能否与装浓硫酸的洗气瓶对调不能(填“能”或“不能”).
③处理尾气的方法可采用在装置末端放一酒精灯将CO燃烧掉(合理均可).(填一种即可).
④某同学用加热高锰酸钾的方法制氧气并用排水法收集,主要的实验步骤有:a 收集氧气 b 装药品 c 熄灭酒精灯 d 固定试管 e 加热 f 移出导管,其中还缺少了一个步骤g,则g是检查装置的气密性,正确顺序为gbdeafc,实验中试管发生破裂,可能的原因是:(任填一条)加热时试管口高于试管底部(合理均可),写出该反应的文字表达式高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
分析 (1)据常用仪器回答;
(2)据反应物状态和反应条件选择发生装置,据氧气的密度和溶解性选择收集装置,据过氧化氢制取氧气的反应原理书写文字表达式;
(3)①据发生装置的选取方法进行选择;
②氧化铜是黑色固体,铜是红色固体,若被还原则固体颜色改变,而一氧化碳还原氧化铜生成二氧化碳,还可据澄清的石灰水变浑浊共同分析判断;气体从溶液中出来会带来水蒸气,所以若将氢氧化钠溶液和浓硫酸对调,则得到的不是干燥的CO;
③CO有毒,所以要将CO收集起来处理再排放,或利用其可燃性将其燃烧掉;
④制取气体的装置在加入药品前要检查装置的气密性,防止装置漏气,并据制取氧气的步骤‘查装定点收移熄’排列正确顺序,据操作分析造成试管破裂的原因,据反应原理书写表达式.
解答 解:(1)标号仪器分别是长颈漏斗和集气瓶;
(2)利用二氧化锰催化双氧水制取氧气不需加热,属于固液常温型,所以选择B发生装置,氧气的密度比空气大且不易溶于水,故可用向上排空气法或排水法收集,反应方程式是:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;
(3)①加热分解草酸晶体属于固体加热型,故选发生装置A;
②根据上面的分析可知:能证明氧化铜被还原的现象是:固体由黑色变为红色,且澄清的石灰水变浑浊;气体从溶液中出来会带来水蒸气,所以若将氢氧化钠溶液和浓硫酸对调,则得到的不是干燥的CO,因此二者不能对调;
③CO有毒,所以要将CO收集起来处理再排放,或利用其可燃性将其燃烧掉;
④制取气体的装置在加入药品前要检查装置的气密性,防止装置漏气,制取氧气的步骤可简记为‘查装定点收移熄’,故正确顺序是:gbdeafc;实验中试管发生破裂,可能的原因有:加热时试管口高于试管底部,未进行预热,用内焰加热,试管外壁有水未擦干就加热,收集完毕先熄灯后移导管等;加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应的文字表达式是:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;
故答案为:(1)长颈漏斗;集气瓶;
(2)B;C(或E);
(3)①A;过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;
②黑色粉末变红,澄清石灰水变浑浊;
③在装置末端放一酒精灯将CO燃烧掉(合理均可);
④检查装置的气密性;gbdeafc;加热时试管口高于试管底部(合理均可);高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
点评 发生装置据反应物状态和反应条件选择,收集装置据气体的密度和溶解性进行选择,并能结合题意及CO的性质等知识灵活分析解答相关问题.

 阅读快车系列答案
阅读快车系列答案| A. | 铝加氧气等于氧化铝 | |
| B. | 铝跟氧气在点燃的条件下,反应生成氧化铝 | |
| C. | 每9份铝在8份氧气中燃烧生成17份氧化铝 | |
| D. | 4个铝原子和6个氧原子等于2个氧化铝分子 |
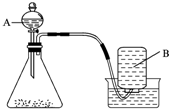 在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾的方法制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.
在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾的方法制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.(1)小明同学选用如图所示的装置制取氧气.制取过程中所发生反应的文字表达式为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
实验前小明同学先向仪器A中加入水,然后将导气管放入水槽中,并打开仪器A的活塞,观察导气管口是否有连续的气泡出现.该实验操作的目的是检查装置的气密性.
(2)实验证明,在过氧化氢溶液中滴加CuSO4溶液能显著加快过氧化氢的分解.CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO4),为了进一步探究CuSO4溶液中哪种粒子能起催化作用,小红同学做了以下分析和设计:
①小红同学认为最不可能的是H2O,她的理由是过氧化氢溶液中的溶剂是水,因此H2O不能起催化作用.
②要说明另外的两种粒子是否起到催化作用,小红同学设计了如下实验,完成了这次探究活动.
| 实验步骤 | 实验现象 | 结论 |
| a.取一支试管加入5mL 5%过氧化氢溶液,然后加入2~3滴稀硫酸溶液 | 溶液几乎没有气泡放出 | 实验证明,起催化作用的是铜离子 |
| b.另取一支试管加入5mL 5%过氧化氢溶液,然后加入2~3滴硫酸铜溶液 | 溶液中有大量气泡放出 |
| A. | 钢铁是钢和铁熔合在一起制得的具有金属特性的合金 | |
| B. | 铁是地壳中含量最丰富的金属元素 | |
| C. | 铝是活泼金属,所以铝制品在空气中易腐蚀 | |
| D. | 铁生锈是铁在有氧气和水等物质存在的条件下,发生复杂的化学反应的过程 |