题目内容
6.调味剂的主要作用是补充、增强或增加食品的味道.食醋是一种能增强食品酸味的调味剂,主要成分为醋酸(CH3COOH),与我们生活密切相联.根据所学知识回答:(1)食醋能作酸味的调味剂,是因为醋酸在水溶液中能解离出CH3COO-,和H+(填离子符号).
(2)食醋的酸味能促进人胃酸的分泌,胃酸的成分是HCl(填化学式).
(3)食醋能软化鱼骨和鸡蛋壳,原因是醋酸能与CaCO3(填化学式)反应.
(4)人体胃酸过多,可用氢氧化铝中和,写出发生反应的化学方程式Al(OH)3+3HCl═AlCl3+3H2O.
分析 (1)根据酸是指在电离时产生的阳离子全部是氢离子的化合物,进行分析解答.
(2)胃酸的成分是盐酸,写出其化学式即可.
(3)鱼骨和鸡蛋壳的主要成分是碳酸钙,能与醋酸反应生成易溶于水的物质,据此进行分析解答.
(4)氢氧化铝和胃酸中的盐酸反应生成氯化铝和水,写出反应的化学方程式即可.
解答 解:(1)食醋能作酸味的调味剂,是因为醋酸在水溶液中能解离出CH3COO-和氢离子,氢离子的离子符号为:H+.
(2)胃酸的成分是盐酸,其化学式为:HCl.
(3)食醋能软化鱼骨和鸡蛋壳,原因是醋酸能与鱼骨和鸡蛋壳的主要成分碳酸钙反应,碳酸钙的化学式为:CaCO3.
(4)氢氧化铝和胃酸中的盐酸反应生成氯化铝和水,反应的化学方程式为:Al(OH)3+3HCl═AlCl3+3H2O.
故答案为:(1)H+;(2)HCl;(3)CaCO3;(4)Al(OH)3+3HCl═AlCl3+3H2O.
点评 本题难度不大,掌握酸的化学性质(能与碱发生中和反应,能与碳酸盐反应等)、化学方程式的书写方法是正确解答本题的关键.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
18.正确的实验操作是进行化学实验的基本保障,下列实验操作正确的是( )
| A. | 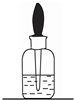 取完液体后,不清洗,直接将胶头滴管放入滴瓶 | |
| B. |  连接试管和胶塞 | |
| C. | 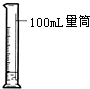 量取9.5mL液体试剂 | |
| D. | 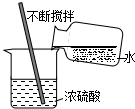 稀释浓硫酸 |
16.天然水经过下列净化操作后,一定能得到饮用纯净水的是( )
| A. | 蒸馏 | B. | 过滤 | C. | 吸附 | D. | 沉淀 |