题目内容
20.己知:甲酸(HCOOH) 常温下是无色易挥发的液体,化学性质与盐酸相似. 甲酸还可以在浓硫酸作用下分解,反应的化学方程式为:HCOOH$→_{△}^{浓硫酸}$CO↑+H2O.某化学兴趣小组的同学利用下列装置制备一氧化碳,并测定某赤铁矿石样品中氧化铁的质量分数.(样品中杂质不参加反应,装置气密性良好,各装置内所装试剂足量)

(1)装置 D 玻璃管中反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)装置 B 的作用是吸收挥发出甲酸气体,防止影响CO2质量的测定,装置C中的试剂是浓硫酸.点燃装置F处酒精灯的目的是将尾气处理,避免造成空气污染.
(3)关于该实验,下列说法正确的是AD
A.开始实验时,先点燃 A 处酒精灯,一段时间后,再点燃 F 处酒精灯
B.实验结束时,熄灭各处酒精灯和喷灯的顺序依次是 A、D、F
C.反应后,装置D玻璃管中的固体物质减少的质量等于E中增加的质量
D.若取赤铁矿石样品质量为m,充分反应后,D中玻璃管内的固体质量减少了n,则样品中氧化铁的质量分数为$\frac{10n}{3m}$×100%
分析 (1)根据化学反应的原理来分析;
(2)根据净化气体的方法以及一氧化碳有毒来分析;
(3)根据实验过程中的注意事项以及反应的过程来分析.
解答 解:(1)一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳.该反应的化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;故填:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)甲酸易挥发,所以B中的氢氧化钠溶液可以吸收挥发出来的甲酸气体,防止对二氧化碳的测定造成影响;C装置内的浓硫酸对一氧化碳气体进行干燥;反应后的尾气中含有有毒的一氧化碳气体,不能直接排放到空气中,为了防止造成空气污染,要对尾气进行点燃处理;故填:吸收挥发出甲酸气体,防止影响CO2质量的测定;浓硫酸;将尾气处理,避免造成空气污染;
(3)A.开始实验时,先点燃A处酒精灯,使产生的一氧化碳排净装置内的空气,一段时间后,再点燃F处酒精灯将尾气点燃,以免造成空气污染,故正确;
B.实验结束时,要先熄灭D处的酒精喷灯,等到装置冷却后再熄灭A处的酒精灯,最后熄灭F处的酒精灯,故错误;
C.装置D玻璃管中的固体物质减少的质量是氧化铁中氧元素的质量,E中增加的质量是反应生成二氧化碳的质量,二者并不相等,故错误;
D.设氧化铁的质量为x,则
3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 固体减少
160 112 160-112=48
x n
$\frac{160}{48}=\frac{x}{n}$
x=$\frac{10}{3}n$
则样品中氧化铁的质量分数为$\frac{\frac{10n}{3}}{m}×100%$=$\frac{10n}{3m}×100%$,故正确.
故填:AD.
点评 本题通过一氧化碳还原氧化铁考查常见物质的性质,增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

| A. | 3.9g | B. | 4g | C. | 7.9g | D. | 16.9g |
| A. | 干冰、空气 | B. | 石灰乳、石油 | C. | 水、金刚石 | D. | 石灰石、纯碱 |
| A. | 组成:均由碳元素和氧元素组成 | |
| B. | 性质:CO2、CO都可以溶于水 | |
| C. | 用途:干冰可用于人工降雨;一氧化碳气体可作燃料 | |
| D. | 危害:二氧化碳含量上升会导致“温室效应”增强;一氧化碳会引起中毒 |
| 选项 | 物质 | 杂质 | 所用试剂 |
| A | 镁粉 | 铁粉 | 稀硫酸 |
| B | N2 | O2 | 灼热的铜网 |
| C | 稀盐酸 | MgCl2 | KOH溶液 |
| D | NaCl | Na2SO4 | Ba(NO3)2溶液 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 大力植树造林 | B. | 使用清洁能源 | C. | 骑自行车出行 | D. | 集中焚烧垃圾 |
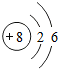 ,Si的元素名称是硅.
,Si的元素名称是硅.