题目内容
2.化学在日常生活中有非常重要的用途,物质的性质往往决定用途,而用途反应出物质的性质.请写出下列应用的化学方程式.(1)电解水的化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(2)天然气(主要成分CH4)充分燃烧的反应CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(3)“斯达舒”【主要成分之一Al(OH)3】可以用于治疗胃酸过多Al(OH)3+3HCl=AlCl3+3H2O;
(4)工业上用稀盐酸去铁制品表面的锈(主要成分为氧化铁)Fe2O3+6HCl═2FeCl3+3H2O;
(5)西汉刘安所述的“曾青得铁则化为铜”的反应Fe+CuSO4═Cu+FeSO4.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答 解:(1)水在通电的条件下生成氢气和氧气,故答案为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(2)天然气(主要成分是CH4),甲烷在点燃条件下燃烧生成二氧化碳和水,反应的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.故答案为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(3)胃舒平[主要成分Al(OH)3]与胃液中的盐酸反应生成氯化铝和水,反应的化学方程式为:Al(OH)3+3HCl=AlCl3+3H2O.
故答案为:Al(OH)3+3HCl=AlCl3+3H2O.
(4)氧化铁与稀盐酸反应生成氯化铁和水.该反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O
故答案为:Fe2O3+6HCl═2FeCl3+3H2O.
(5)曾青得铁则化为铜,曾青是铜的化合物,即用铁将铜的化合物中的铜置换出来,反应物是铁和硫酸铜溶液,生成物是硫酸亚铁溶液和铜,反应的化学方程式为:Fe+CuSO4═Cu+FeSO4.
故答案为:Fe+CuSO4═Cu+FeSO4
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案
相关题目
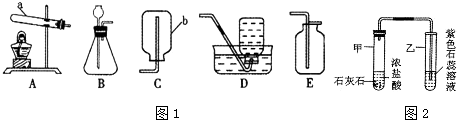
10.化学是一门以实验为基础的科学,许多化学重大发现和研究成果都是通过实验得到的.下列实验操作中,符合操作规范的是( )
| A. | 在实验室用100mL量筒准确量取8.5mL盐酸 | |
| B. | 点燃氢气前,一定要先检验氢气的纯度 | |
| C. | 稀释浓硫酸时,将水倒入盛浓硫酸的烧杯中 | |
| D. | 测定某溶液的pH时,先要用水湿润pH试纸 |
17.将洁净的铜丝浸入含有AgNO3和Zn(NO3)2的混合液中,一段时间后,铜丝表面覆盖了一层固体物质,这层物质是下列的( )
| A. | 只有Zn | B. | 只有Ag | C. | Zn和Ag | D. | Zn和Cu |
7.下列属于化学变化的是( )
| A. | 从海水中获得物质 | |
| B. | 用石灰浆粉刷墙壁,干燥后墙面变硬 | |
| C. | 石油分馏后得到汽油、煤油、柴油 | |
| D. | 潮湿的衣服被晒干 |
14.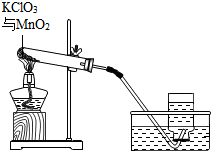 某兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据如表.制取结束后,将剩余固体用矢量水充分溶解后,过滤,回收二氧化锰固体.
某兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据如表.制取结束后,将剩余固体用矢量水充分溶解后,过滤,回收二氧化锰固体.
(1)共制得氧气9.6g.
(2)计算原混合物中二氧化锰的质量.
 某兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据如表.制取结束后,将剩余固体用矢量水充分溶解后,过滤,回收二氧化锰固体.
某兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据如表.制取结束后,将剩余固体用矢量水充分溶解后,过滤,回收二氧化锰固体. | 加热时间/min | 0 | t1 | t2 | t3 |
| 固体质量/g | 28.0 | 23.2 | 18.4 | 18.4 |
(2)计算原混合物中二氧化锰的质量.
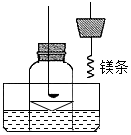 某科学兴趣小组查阅资料得知镁可在氮气中燃烧生成氮化镁(Mg3N2),设计了如下方案进行验证.
某科学兴趣小组查阅资料得知镁可在氮气中燃烧生成氮化镁(Mg3N2),设计了如下方案进行验证.