题目内容
6.有关酸和碱的说法不正确的是( )| A. | 不是所有的酸和碱都能发生中和反应 | |
| B. | 酸在水中解离出来的阳离子全部是H+ | |
| C. | 酸碱中和反应的实质是H+与OH-结合生成水 | |
| D. | 碱有共同的化学性质是因为有OH- |
分析 A、中和反应属于复分解反应,结合复分解反应发生的条件进行分析判断.
B、根据酸具有相似化学性质的原因,进行分析判断.
C、根据中和反应的实质进行分析判断.
D、根据碱具有相似化学性质的原因,进行分析判断.
解答 解:A、中和反应属于复分解反应,不是所有的酸和碱都能发生中和反应,如难溶性的酸与难溶性的碱不能发生中和反应,故选项说法错误.
B、酸在水中解离出来的阳离子全部是H+,故选项说法正确.
C、酸碱中和反应的实质是H+与OH-结合生成水,故选项说法正确.
D、碱有共同的化学性质是因为解离出来的阴离子全部是OH-,而不是因为有OH-,故选项说法错误.
故选:D.
点评 本题难度不大,掌握中和反应及其实质、酸与碱具有通性的原因等是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.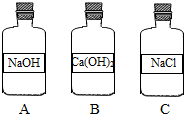 同学们在清理实验室时,发现如图三个内壁都有白色固体的细口瓶,请你和同学们一起完成清洗和以下探究活动.
同学们在清理实验室时,发现如图三个内壁都有白色固体的细口瓶,请你和同学们一起完成清洗和以下探究活动.
(1)三个瓶中的白色固体一定是纯净物的是NaCl(填化学式).
(2)只用水不能清洗干净的细口瓶是B(填“A”或“B”或“C”).
(3)探究B瓶中白色固体的成分.
【提出问题】B中白色固体是什么物质?
【猜想与假设】
猜想1:可能是CaCO3 猜想2:可能是Ca(OH)2 猜想3:可能是 CaCO3和Ca(OH)2的混合物.
【设计实验】
①甲同学取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解.于是他得出粉末中一定有CaCO3的结论.乙同学查阅了溶解性表(如下表),认为甲同学的结论不严密,理由是:Ca(OH)2微溶于水也可能不溶解而沉淀.
②为了得出较严密的结论,他们进行了如下实验,请完成下列实验报告:
(4)最后用稀盐酸和水将三个细口瓶洗净,洗后液体倒入一个干净的容器中,得到澄清无色溶液,写出其中一定含有的溶质NaCl、CaCl2.
 同学们在清理实验室时,发现如图三个内壁都有白色固体的细口瓶,请你和同学们一起完成清洗和以下探究活动.
同学们在清理实验室时,发现如图三个内壁都有白色固体的细口瓶,请你和同学们一起完成清洗和以下探究活动.(1)三个瓶中的白色固体一定是纯净物的是NaCl(填化学式).
(2)只用水不能清洗干净的细口瓶是B(填“A”或“B”或“C”).
(3)探究B瓶中白色固体的成分.
【提出问题】B中白色固体是什么物质?
【猜想与假设】
猜想1:可能是CaCO3 猜想2:可能是Ca(OH)2 猜想3:可能是 CaCO3和Ca(OH)2的混合物.
【设计实验】
①甲同学取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解.于是他得出粉末中一定有CaCO3的结论.乙同学查阅了溶解性表(如下表),认为甲同学的结论不严密,理由是:Ca(OH)2微溶于水也可能不溶解而沉淀.
| OHˉ | Clˉ | CO32ˉ | NO3ˉ | |
| Ca2+ | 微溶 | 溶 | 不 | 溶 |
| 实验步骤 | 可能观察到的现象 | 结论 |
| 取上述试管中的上层清液,滴加1-2滴无色酚酞试液 | ||
| 往上述试管中的残留的固体中加入稀盐酸 | 白色粉末中有(填“有”或“无”)CaCO3 |
14.某同学描述的有关实验现象如下,你认为正确的是( )
| A. | 硫在氧气中燃烧产生微弱的淡蓝色火焰,并生成有刺激性气味的气体 | |
| B. | 点燃棉制品时时产生烧焦羽毛的气味 | |
| C. | 将CO通入到灼热的氧化铜中,发现红色粉末立即变成黑色 | |
| D. | 将澄清的饱和石灰水加热,发现有白色浑浊出现 |
11.某学习小组的同学们在做氢氧化钠溶液和稀硫酸的中和反应实验中,突然发现未给烧杯中滴加指示剂.于是将实验改为探究烧杯内的溶液中溶质的成分.
【提出问题】烧杯内的溶液中溶质是什么?
【猜想与假设】同学们经过讨论,一致认为溶质一定有硫酸钠,写出生成硫酸钠的化学方程式2NaOH+H2SO4=Na2SO4+2H2O.溶质除了硫酸钠外,小敏同学认为还可能有氢氧化钠,小丽同学认为还可能有硫酸.
【查阅资料】硫酸钠溶液呈中性.
【设计与实验】
(1)同学们取少量烧杯中的溶液于试管中,滴加酚酞溶液,无明显现象产生,据此推断小敏同学的猜想不成立,理由是酚酞溶液没有变红,溶液中没有氢氧化钠.
(2)小丽同学取少量烧杯中的溶液于试管中,滴加氯化钡溶液,有白色沉淀生成,她据此确定溶质还有硫酸.反应的化学方程式为BaCl2+H2SO4=BaSO4↓+2HCl.
(3)小华同学提出质疑,因为溶液中的硫酸钠与氯化钡反应也能产生白色沉淀.为了证明溶质是否还有硫酸,请你与同学们一起进行如表探究.
【反思与评价】
(1)在探究化学反应后的剩余物质的成分是,除了考虑生成物,还要考虑反应物的用量.
(2)复分解反应发生的条件是生成物中有沉淀或有气体或有水生成.
【提出问题】烧杯内的溶液中溶质是什么?
【猜想与假设】同学们经过讨论,一致认为溶质一定有硫酸钠,写出生成硫酸钠的化学方程式2NaOH+H2SO4=Na2SO4+2H2O.溶质除了硫酸钠外,小敏同学认为还可能有氢氧化钠,小丽同学认为还可能有硫酸.
【查阅资料】硫酸钠溶液呈中性.
【设计与实验】
(1)同学们取少量烧杯中的溶液于试管中,滴加酚酞溶液,无明显现象产生,据此推断小敏同学的猜想不成立,理由是酚酞溶液没有变红,溶液中没有氢氧化钠.
(2)小丽同学取少量烧杯中的溶液于试管中,滴加氯化钡溶液,有白色沉淀生成,她据此确定溶质还有硫酸.反应的化学方程式为BaCl2+H2SO4=BaSO4↓+2HCl.
(3)小华同学提出质疑,因为溶液中的硫酸钠与氯化钡反应也能产生白色沉淀.为了证明溶质是否还有硫酸,请你与同学们一起进行如表探究.
| 实验步骤 | 实验现象 | 实验结论 |
取少量烧杯中的溶液于试管中,加入锌粒 | 有气泡产生 | 溶质还有硫酸 |
(1)在探究化学反应后的剩余物质的成分是,除了考虑生成物,还要考虑反应物的用量.
(2)复分解反应发生的条件是生成物中有沉淀或有气体或有水生成.
18.如图图象能正确反映对应的实验操作的是( )
| A. | 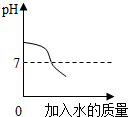 把水加到NaOH溶液中 把水加到NaOH溶液中 | |
| B. | 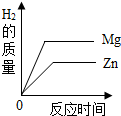 等质量的Mg和Zn与足量的稀硫酸反应,产生H2的质量 等质量的Mg和Zn与足量的稀硫酸反应,产生H2的质量 | |
| C. | 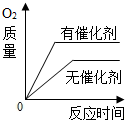 用一定量的双氧水制取氧气 用一定量的双氧水制取氧气 | |
| D. | 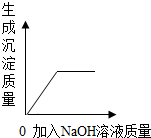 向硫酸和硫酸铜的混合溶液中滴加过量的NaOH溶液 向硫酸和硫酸铜的混合溶液中滴加过量的NaOH溶液 |
15.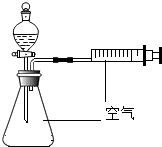 如图装置的分液漏斗和锥形瓶中所盛的药品如表所示(不考虑针管内部的摩擦力):
如图装置的分液漏斗和锥形瓶中所盛的药品如表所示(不考虑针管内部的摩擦力):
滴入分液漏斗中的液体,记录注射器活塞的位置,一段时间后,可观察到注射器的活塞向左移动的是( )
 如图装置的分液漏斗和锥形瓶中所盛的药品如表所示(不考虑针管内部的摩擦力):
如图装置的分液漏斗和锥形瓶中所盛的药品如表所示(不考虑针管内部的摩擦力):| 编号 | 分液漏斗 | 锥形瓶 |
| ① | 食盐水 | 铁钉 |
| ② | H2O2水溶液 | 二氧化锰固体 |
| ③ | NaOH溶液 | FeSO4溶液 |
| ④ | 蒸馏水 | 火碱固体 |
| A. | ①② | B. | 只有① | C. | ①③ | D. | ②④ |
16.下列事实与对应的解释相符的是( )
| A. | 空气能被压缩--分子体积可以变小 | |
| B. | 50mL水和50mL酒精混合后的总体积小于100mL--分子质量小 | |
| C. | 结冰的水不能流动--0℃以下,水分子不再运动 | |
| D. | 甘蔗甜,苦瓜苦--构成物质的分子不同 |