题目内容
6.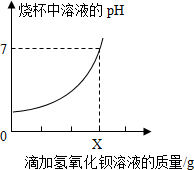 测定某品牌洁厕灵中硫酸质量.取20g该品牌的洁厕灵溶液于烧杯中,不断滴加25g溶质质量分数为17.1%的氢氧化钡溶液,反应过程中滴入氢氧化钡溶液的质量和烧杯中溶液pH变化的部分数据如表所示:
测定某品牌洁厕灵中硫酸质量.取20g该品牌的洁厕灵溶液于烧杯中,不断滴加25g溶质质量分数为17.1%的氢氧化钡溶液,反应过程中滴入氢氧化钡溶液的质量和烧杯中溶液pH变化的部分数据如表所示:| 滴加氢氧化钡溶液的质量/g | 5 | 10 | X | 25 |
| 烧杯中产生沉淀的质量/g | 1.165 | 2.33 | 4.66 | 4.66 |
①当烧杯中溶液的pH=7时,加入氢氧化钡溶液质量X=20g.
②测得20g该品牌的洁厕灵溶液中硫酸的质量是1.96g.(根据化学方程式计算)
分析 ①根据表中信息可知:每加5g氢氧化钡溶液,可以产生1.165g沉淀,产生4.66g沉淀需要消耗氢氧化钡溶液20g;
②硫酸与氢氧化钡溶液反应生成硫酸钡沉淀和水,根据产生的沉淀的质量为4.66g,据此结合反应的化学方程式进行分析解答即可.
解答 解:
①根据表中信息可知:每加5g氢氧化钡溶液,可以产生1.165g沉淀,故产生4.66g沉淀需要消耗氢氧化钡溶液20g;
②由题意可知:产生4.66g沉淀需要消耗氢氧化钡溶液20g,此时硫酸完全反应,设该20g稀H2SO4溶液中溶质为x.
Ba(OH)2+H2SO4=BaSO4↓+2H2O
98 233
x 4.66g
则$\frac{98}{233}=\frac{x}{4.66g}$,解得x=1.96g.
故测得20g该品牌的洁厕灵溶液中硫酸的质量是1.96g.
故答案为:
①20g;②1.96g.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,细致地分析题中信息,根据找出生成硫酸钡沉淀的质量是正确解答本题的前提和关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.2016年4月22日是第47个世界地球日,主题是“节约利用资源,倡导绿色生活”.下列做法符合这一主题的是( )
| A. | 大量砍伐树木,代替煤作燃料 | |
| B. | 用焚烧秸秆的灰烬给庄稼补充钾肥 | |
| C. | 鼓励燃煤发电,实现区域电力互惠互享 | |
| D. | 自带布袋去农贸市场,减少使用一次性塑料袋 |
17.下列关于O2的说法正确的是( )
①表示氧元素;
②表示一个氧分子;
③表示两个氧原子;
④表示氧气由氧元素组成;
⑤表示两个氧分子;
⑥表示一个氧分子由两个氧原子构成.
①表示氧元素;
②表示一个氧分子;
③表示两个氧原子;
④表示氧气由氧元素组成;
⑤表示两个氧分子;
⑥表示一个氧分子由两个氧原子构成.
| A. | ①②③ | B. | ②④⑥ | C. | ②④⑤ | D. | ④⑤⑥ |
1.汽车尾气中主要含有NO、CO等气体,为减轻污染给车安装“三效催化净化器”,反应为:2CO+2NO$\stackrel{催化剂}{→}$ N2+2CO2,其中发生还原反应的是( )
| A. | NO | B. | CO | C. | N2 | D. | CO2 |
11.在硝酸银、硝酸铜的混合溶液中加入一定量铁粉,反应停止后过滤,滤渣中加入盐酸,无气泡产生.有关判断正确的是( )
| A. | 滤渣中一定有银,没有铁和铜 | |
| B. | 滤渣中一定有铜,可能有铁和银 | |
| C. | 滤液中一定有硝酸亚铁、硝酸铜,没有硝酸银 | |
| D. | 滤液中一定有硝酸亚铁,可能有硝酸铜和硝酸银 |
18.随着车辆的增加,汽车尾气带给城市的污染越来越严重了,用燃气来代替燃油可以大大减少汽车尾气的污染.某市的加气站某日发生了爆炸,请你分析爆炸的原因.为防止此类事件的再次发生,请你提出一条合理化建议.
11.已知过氧化钠的化学式为Na2 O2;则关于过氧化钠的说法正确的是( )
| A. | 由两个钠元素和两个氧元素组成 | B. | 由氧化钠分子和氧原子构成 | ||
| C. | 由钠元素和氧元素组成 | D. | 由两个钠原子和氧原子构成 |
 稀HCl和NaOH溶液反应时的溶液酸碱度变化如图所示
稀HCl和NaOH溶液反应时的溶液酸碱度变化如图所示