题目内容
12.有①Cu-Zn ②Cu-Ag 两种貌似黄金的合金,它们都有其特殊的用途,但一些骗子常用它们做成饰品冒充真黄金欺骗消费者.对此,化学科学有责任加以揭露.(1)现有上述两种合金制成的假黄金饰品各一件,小明同学只用稀盐酸和必要的实验仪器就鉴别出其中一种饰品是假黄金,它是合金①(填写代号);若要证明另一种饰品也是假黄金,可选用一种盐溶液来验证,这种盐可以是硝酸银或AgNO3(写一种盐的名称或化学式);
(2)取与上述用稀盐酸鉴别出的同种合金10g,放入烧杯中,再向其中加入93.7g某稀盐酸恰好完全反后,测得烧杯内剩余物质的质量共为103.5g.
①上述过程中变化的质量10g,+93.7g-103.5g=0.2g是氢气或H2(填物质的名称或化学式)的质量;
②10g,该合金中铜的质量是多少?已知反应后的溶液中溶质全部溶解,求该溶液中溶质的质量分数是多少?
分析 锌能和稀盐酸反应生成氯化锌和氢气,铜不能和稀盐酸反应;
铜能和稀盐酸反应生成硝酸铜和银;
根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:(1)只用稀盐酸和必要的实验仪器就鉴别出其中一种饰品是假黄金,它是铜锌合金,因为其中的锌能和稀盐酸反应生成氯化锌和氢气;
若要证明另一种饰品也是假黄金,可选用一种盐溶液来验证,这种盐可以是硝酸银,因为硝酸银能和铜反应生成硝酸铜和银.
故填:①;硝酸银或AgNO3.
(2)①上述过程中变化的质量10g,+93.7g-103.5g=0.2g是氢气或H2的质量.
故填:氢气或H2.
②设锌的质量为x,生成氯化锌质量为y,
Zn+2HCl═ZnCl2+H2↑,
65 136 2
x y 0.2g
$\frac{65}{x}$=$\frac{136}{y}$=$\frac{2}{0.2g}$,
x=6.5g,y=13.6g,
该合金中铜的质量是:10g-6.5g=3.5g,
该溶液中溶质的质量分数是:$\frac{13.6g}{6.5g+93.7g-0.2g}$×100%=13.6%,
答:该合金中铜的质量是3.5g,该溶液中溶质的质量分数是13.6%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
3.在公共场所,利用“活性炭+超滤膜+紫外线”组合工艺可获得直饮水,其中活性炭的主要作用是( )
| A. | 还原 | B. | 吸附 | C. | 导电 | D. | 消毒 |
20.磷酸二氢铵(NH4H2PO4)是农业上一种常用的化肥.下列叙述正确的是( )
| A. | 磷酸二氢铵属于氮肥 | |
| B. | 磷酸二氢铵中,氮、氢、磷、氧元素的质量比是1:6:1:4 | |
| C. | 磷酸二氢铵的相对分子质量是115 | |
| D. | 磷酸二氢铵是一种氧化物 |
17.密闭容器内有四种物质,测得反应前后各物质的质量如下表:下列说法正确的是( )
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量∕g | 8 | 2 | 40 | 5 |
| 反应后质量∕g | 待测 | 24 | 8 | 23 |
| A. | 该反应一定是置换反应 | |
| B. | 乙和丁的相对分子质量比一定为11:9 | |
| C. | 参加反应的甲、丙的质量比为1:4 | |
| D. | 反应后甲的质量为8克 |
1.粗盐提纯实验的部分操作如图所示,其中错误的是( )
| A. |  取样 | B. |  溶解 | C. |  过滤 | D. |  蒸发 |
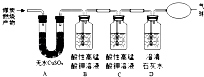 我国是世界上最大的煤炭生产国和消费国,也是世界上少数几个以煤炭为主要能源的国家之一.化学兴趣小组的同学对煤炭燃烧的主要产物产生了兴趣,请你参与:
我国是世界上最大的煤炭生产国和消费国,也是世界上少数几个以煤炭为主要能源的国家之一.化学兴趣小组的同学对煤炭燃烧的主要产物产生了兴趣,请你参与: