题目内容
5.修建铁路所需大量钢铁是以铁矿石为主要原料冶炼而得.(1)写出用一氧化碳和赤铁矿炼铁的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)雨后的铁轨表面易产生少量的锈迹,这是因为铁在潮湿的空气中易生锈;
(3)实验室可用盐酸除铁锈,其化学方程式为Fe2O3+6HCl═2FeCl3+3H2O;
(4)铝热剂是修建铁路时常用的焊接材料,其反应原理是铝在一定条件下与氧化铁反应得到熔融的铁与另一种氧化物,该反应基本类型是置换反应.
分析 (1)高温条件下,一氧化碳和氧化铁反应生成铁和二氧化碳.
(2)铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果.
(3)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,写出反应的化学方程式即可.
(4)铝在一定条件下与氧化铁反应得到融熔的铁与另一种氧化物,由质量守恒定律,反应前后元素种类不变,该氧化物是氧化铝,据此进行分析解答.
解答 解:(1)高温条件下,一氧化碳和氧化铁反应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)雨后的铁轨表面易产生少量的锈迹,这是因为雨后空气中水蒸气含量较多,铁在潮湿的空气中易生锈.故填:铁在潮湿的空气中易生锈;
(3)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O.故填:Fe2O3+6HCl=2FeCl3+3H2O;
(4)铝在一定条件下与氧化铁反应得到融熔的铁与另一种氧化物,由质量守恒定律,反应前后元素种类不变,该氧化物是氧化铝,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.故填:置换反应.
点评 本题难度不大,掌握一氧化碳还原氧化铁的反应原理、铁锈蚀的条件、置换反应的特征等是正确解答本题的关键.

练习册系列答案
相关题目
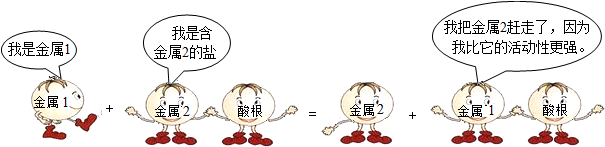
10.下列四个化学反应中,符合此漫画情景的是( )

| A. | Cu+2AgCl═Ag+CuCl2 | B. | Fe+H2S04═FeS04+H2↑ | ||
| C. | H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H20 | D. | Fe+CuS04═FeS04+Cu |
17.日常生活中,区别下列各组物质所用的方法,正确的是( )
| A. | 白酒和白醋--观察颜色 | B. | 棉线和羊毛线--灼烧,闻气味 | ||
| C. | 黄铜和黄金--观察颜色 | D. | 食盐和苏打--加水,观察是否溶解 |
 铁是常用的金属材料.兴趣小组的同学对某铁制品中铁的质量分数进行了测定. 称取3g铁屑,缓慢加入一定溶质质量分数的硫酸溶液,直到过量(假设除铁以外的物质都不与硫酸反应),实验数据如图所示. 请计算:
铁是常用的金属材料.兴趣小组的同学对某铁制品中铁的质量分数进行了测定. 称取3g铁屑,缓慢加入一定溶质质量分数的硫酸溶液,直到过量(假设除铁以外的物质都不与硫酸反应),实验数据如图所示. 请计算: 如图是某同学对二氧化碳部分知识构建的网络图,请根据图中信息填空.
如图是某同学对二氧化碳部分知识构建的网络图,请根据图中信息填空.