题目内容
2.(南海是我国的固有领海,南海蕴藏着丰富的海洋资源).(1)我国科学家在南海海底发现了一种蕴藏量极大的新型矿产资源--天然气水合物,它是天然气(主要成分是CH4)和水形成的冰状固体,极易燃烧,又称“可燃冰”.它被认为是一种清洁能源,原因是燃烧产物是水和二氧化碳,不污染环境.
(2)从海水中提取单质镁的过程如图1所示:

在上述转化过程中,所发生的化学反应属于复分解反应的是①②(填反应顺序标号).
(3)我国化学科学家侯德榜创立的侯氏制碱法,就是以海水“晒盐”得到的氯化钠为原料,同时制得Na2CO3和NH4Cl产品.Na2CO3和NH4Cl的溶解度曲线如图2所示.回答下列问题:
①t1℃时,NH4Cl的溶解度大于Na2CO3的溶解度(填“大于”“小于”“等于”之一).
②t2℃时,Na2CO3饱和溶液的溶质质量分数等于NH4Cl饱和溶液的溶质质量分数(填“大于”“小于”“等于”之一).
③t1℃时,一小试管内盛有Na2CO3的饱和溶液,试管底部还存有少许Na2CO3固体,将小试管放入盛有水的烧杯中,现将多 量的NaOH固体加入烧杯内的水中,小试管内的固体物质逐渐溶解,原因是氢氧化钠溶于水放出热量,温度升高,碳酸钠的溶解度增大,变为不饱和溶液,所以又能溶解碳酸钠了.
分析 (1)根据可燃冰的优点考虑;
(2)根据复分解反应的特点:两种化合物相互交换成分生成两种新的化合物的反应类型;
(3)①根据某一温度时物质溶解度的比较方法考虑;②根据饱和溶液的质量分数的计算考虑;③根据氢氧化钠溶于水放热考虑.
解答 解:(1)因为可燃冰燃烧放出的热量多,燃烧产物是二氧化碳和水,不污染环境所以被认为是一种清洁能源;
(2)第①个反应是氯化镁与氢氧化钙反应生成氢氧化镁沉淀和氯化钙,属于复分解反应,第②是氢氧化镁与盐酸反应生成氯化镁和水,属于复分解反应;
(3)①从t1℃向上做垂线,与曲线的交点在上面的溶解度就大,所以t1℃时,NH4Cl的溶解度大于Na2CO3的溶解度;
②饱和溶液的质量分数:$\frac{溶解度}{溶解度+100g}$×100%,又因为t2℃时,Na2CO3的溶解度等于NH4Cl的溶解度,所以饱和溶液的质量分数也相等;
③氢氧化钠溶于水放热,所以使溶液温度升高,碳酸钠的溶解度增大,变为不饱和溶液,所以又能溶解碳酸钠了.
故答案为:(1)燃烧产物是水和二氧化碳,不污染环境;(2)①②;(3)①大于;②等于;③氢氧化钠溶于水放出热量,温度升高,碳酸钠的溶解度增大,变为不饱和溶液,所以又能溶解碳酸钠了.
点评 解答本题关键是要知道可燃冰的燃烧产物,复分解反应的定义,溶解度大小的判断,饱和溶液的质量分数的计算.

练习册系列答案
相关题目
4.现有Mg(OH)2和MgCO3的固体混合物6g,经测定镁元素的质量分数为40%,向固体混合物中加入100g一定溶质质量分数的稀盐酸,恰好完全反应,下列说法不正确的是( )
| A. | 反应过程中有气泡产生 | |
| B. | 生成MgCl2的质量为9.5g | |
| C. | 反应后溶液中的溶质只有MgCl2 | |
| D. | 所用稀盐酸中溶质的质量分数为14.6% |
10.下列过程中,一定涉及化学变化的是( )
| A. | 石油分馏得到汽油 | B. | 用食醋除去水壶中的水垢 | ||
| C. | 蒸馏水淡化海水 | D. | 过滤除去食盐水中的泥沙 |
17. 小明同学在实验室中进行如下实验,请你和他一起完成.
小明同学在实验室中进行如下实验,请你和他一起完成.
(1)配制100g质量分数为20%的氢氧化钠溶液,他应称量的氢氧化钠固体质量为20g.配制过程中应用到的玻璃仪器有:量筒、烧杯、玻璃棒,称量氢氧化钠时,应将其放入玻璃器皿中称量,这是因为氢氧化钠具有吸水性且其水溶液具有强烈的腐蚀性.经精确测定,小明配制的溶液溶质质量分数小于20%,你认为其可能的原因是(写一条)使用量筒读数时仰视.
(2)小明取部分配制好的溶液做了如图所示的实验(其他仪器已略去):反应的化学方程式为CO2+2NaOH═Na2CO3+H2O.
(3)通入一段时间CO2后,小明想对试管中的溶液组成进行探究.
【提出问题】溶液中的溶质有哪些物质?
【猜想】Ⅰ:只有氢氧化钠;
Ⅱ、既有氢氧化钠又有碳酸钠;
Ⅲ、只有碳酸钠.
【查阅资料】CaCl2溶液呈中性,能与碳酸钠溶液反应生成碳酸钙沉淀和氯化钠.
【实验探究】小明设计了如下实验进行验证,请完成下表中的空格.
【反思与评价】实验②、③中都滴入了稍过量的CaCl2稀溶液,其目的是:可以完全除去碳酸钠,可否用稀盐酸替代CaCl2溶液?理由是不可以,盐酸可以和碳酸钠和氢氧化钠反应.
 小明同学在实验室中进行如下实验,请你和他一起完成.
小明同学在实验室中进行如下实验,请你和他一起完成.(1)配制100g质量分数为20%的氢氧化钠溶液,他应称量的氢氧化钠固体质量为20g.配制过程中应用到的玻璃仪器有:量筒、烧杯、玻璃棒,称量氢氧化钠时,应将其放入玻璃器皿中称量,这是因为氢氧化钠具有吸水性且其水溶液具有强烈的腐蚀性.经精确测定,小明配制的溶液溶质质量分数小于20%,你认为其可能的原因是(写一条)使用量筒读数时仰视.
(2)小明取部分配制好的溶液做了如图所示的实验(其他仪器已略去):反应的化学方程式为CO2+2NaOH═Na2CO3+H2O.
(3)通入一段时间CO2后,小明想对试管中的溶液组成进行探究.
【提出问题】溶液中的溶质有哪些物质?
【猜想】Ⅰ:只有氢氧化钠;
Ⅱ、既有氢氧化钠又有碳酸钠;
Ⅲ、只有碳酸钠.
【查阅资料】CaCl2溶液呈中性,能与碳酸钠溶液反应生成碳酸钙沉淀和氯化钠.
【实验探究】小明设计了如下实验进行验证,请完成下表中的空格.
| 编号 | 实验操作 | 实验现象 | 实验结论 |
| ① | 取试管中溶液少许,滴入适量的稀盐酸 | 有气泡产生 | 猜想Ⅰ错误. |
| ② | 取试管中溶液少许,滴入稍过量的CaCl2稀溶液,过滤后,向澄清滤液中滴入无色酚酞试液 | 溶液变浑浊,有沉淀产生,溶液变成红色. | 猜想Ⅱ正确. |
| ③ | 取试管中溶液少许,滴入稍过量的CaCl2稀溶液,过滤后,向滤液中加入滴入无色酚酞试液. | 澄清滤液中加入试液后,无明显现象. | 猜想Ⅲ正确. |
12.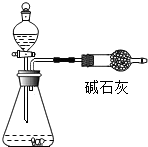 同学们想测定一定质量的石灰石中CaCO3质量分数,他们设计了如图的实验装置(碱石灰的成分是CaO和NaOH的混合物),利用测定碱石灰质量增加来计算碳酸钙的质量.
同学们想测定一定质量的石灰石中CaCO3质量分数,他们设计了如图的实验装置(碱石灰的成分是CaO和NaOH的混合物),利用测定碱石灰质量增加来计算碳酸钙的质量.
(1)该装置导致实验结果偏大的可能原因是BCD.
A.装置内残留的CO2气体不能全部排出.
B.产生的CO2气体中混有氯化氢气体,同时被碱石灰吸收.
C.产生的CO2气体中混有水蒸气,同时被碱石灰吸收.
D.球形干燥管与空气相通,也会吸收空气中的CO2和H2O.
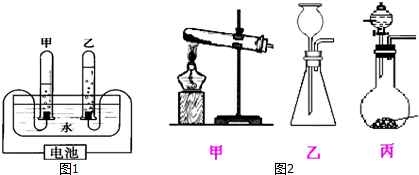
(2)做完上述实验后,同学们对反应后反应器内的剩余溶液的溶质成分产生了兴趣,他们继续进行了以下实验探究:将剩余的溶液倒入烧杯中,微热后冷却到室温.
上表甲、乙、丙三个同学的实验操作中有错误的是丙(选填“甲”“乙”或“丙”)同学的方案.
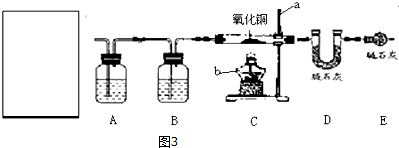
 同学们想测定一定质量的石灰石中CaCO3质量分数,他们设计了如图的实验装置(碱石灰的成分是CaO和NaOH的混合物),利用测定碱石灰质量增加来计算碳酸钙的质量.
同学们想测定一定质量的石灰石中CaCO3质量分数,他们设计了如图的实验装置(碱石灰的成分是CaO和NaOH的混合物),利用测定碱石灰质量增加来计算碳酸钙的质量.(1)该装置导致实验结果偏大的可能原因是BCD.
A.装置内残留的CO2气体不能全部排出.
B.产生的CO2气体中混有氯化氢气体,同时被碱石灰吸收.
C.产生的CO2气体中混有水蒸气,同时被碱石灰吸收.
D.球形干燥管与空气相通,也会吸收空气中的CO2和H2O.
(2)做完上述实验后,同学们对反应后反应器内的剩余溶液的溶质成分产生了兴趣,他们继续进行了以下实验探究:将剩余的溶液倒入烧杯中,微热后冷却到室温.
| 实验操作 | 实验现象 | 实验结论 | |
甲同学 | 取烧杯中溶液少许于试管中,向其中滴加紫色石蕊试液 | 现象:溶液变为红色 | 溶液显酸性(含有H+);溶质中有氯化氢. |
乙同学 | 取烧杯中溶液少许于试管中,向其中加入少量锌粒 | 现象:产生气泡,反应的化学方程式是: Zn+2HCl═ZnCl2+H2↑ | |
丙同学 | 取烧杯中溶液少许于试管中,向其中加入少量硝酸银溶液 | 现象:产生白色沉淀 |
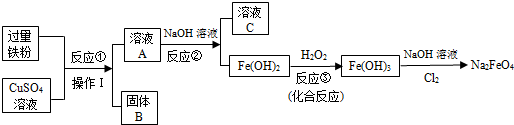
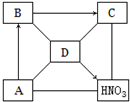 A、B、C、D四种物质分别是酸碱盐和氧化物中的一种,其中有一种是胃液的主要成分,B是一种常用的食品干燥剂.它们之间的转化关系如图所示,“-”表示相互反应,“→”表示相互转化.请回答:
A、B、C、D四种物质分别是酸碱盐和氧化物中的一种,其中有一种是胃液的主要成分,B是一种常用的食品干燥剂.它们之间的转化关系如图所示,“-”表示相互反应,“→”表示相互转化.请回答: