题目内容
7.用金属铁制备自来水新型消毒、净水剂Na2FeO4的流程如图,请回答下列问题: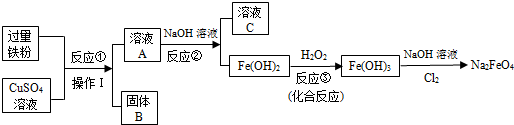
(1)溶液A的溶质是硫酸亚铁(写名称);写出Na2FeO4中铁元素的化合价+6.
(2)操作Ⅰ用到玻璃棒的作用是引流.
(3)请写出反应2的化学方程式:FeSO4+2NaOH=Fe(OH)2↓+Na2SO4,反应类型是复分解反应.
分析 (1)根据反应①过量铁粉与硫酸铜的反应分析固体B的成分,根据化合价原则“化合物中各元素的化合价的代数和为0”,由化学式求出元素的化合价;
(2)根据过滤可用于固体和液体的分离以及过滤的所需的仪器进行解答;
(3)根据发生的反应写出反应的化学方程式.
解答 解:(1)由反应的流程可知,过量的铁粉与硫酸铜反应,生成了硫酸亚铁和铜,故溶液A的溶质是硫酸亚铁;在K2FeO4中,由于钾元素显+1价、氧显-2价,设铁的化合价为x,由化合价原则可知:(+1)×2+x+(-2×4)=0,解得:x=+6.
(2)由上述反应①得到是固液的混合物,要将固液分开,应进行的操作是过滤,过滤时玻璃棒的作用是引流;
(3)由反应的流程可知:反应②是硫酸亚铁与氢氧化钠反应,方程式是:FeSO4+2NaOH=Fe(OH)2↓+Na2SO4;属于复分解反应;
故答案为:
(1)硫酸亚铁;+6.(2)引流.(3)FeSO4+2NaOH=Fe(OH)2↓+Na2SO4,复分解反应.
点评 本题给出了制取物质的反应流程图,对于这类题目,需要搞清楚每一步反应物、生成物,清楚工艺流程原理.再结合有关的知识分析解答有关的问题.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
12.下列做法或认识科学的是( )
| A. | 厨房煤气泄漏,立即打开排气扇电源 | |
| B. | 用软水洗衣服比用硬水洗效果好 | |
| C. | 防煤气中毒,煤炉上放 盆水 | |
| D. | 寻找一种催化剂将水变为汽油 |
17.下列有关溶液的说法正确的是( )
| A. | 降低饱和溶液的温度,一定有晶体析出 | |
| B. | 长期放置后不会分层的液体不一定是溶液 | |
| C. | 硝酸钾饱和溶液一定比其不饱和溶液质量分数大 | |
| D. | 配制好6%的NaCl溶液,装瓶时不小心撒漏一部分,瓶中NaCl溶液浓度小于6% |
 如图是初中化学中常见物质间的转化关系,其中甲、乙为单质,A、B、C、D为化合物,且A与B的组成元素相同,C与D的组成元素也相同.其余反应条件、部分反应物已略去.试判断:
如图是初中化学中常见物质间的转化关系,其中甲、乙为单质,A、B、C、D为化合物,且A与B的组成元素相同,C与D的组成元素也相同.其余反应条件、部分反应物已略去.试判断:
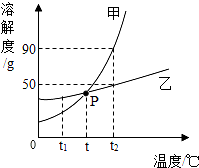 如图为甲、乙两种物质的溶解度曲线,据图回答下列问题.
如图为甲、乙两种物质的溶解度曲线,据图回答下列问题.